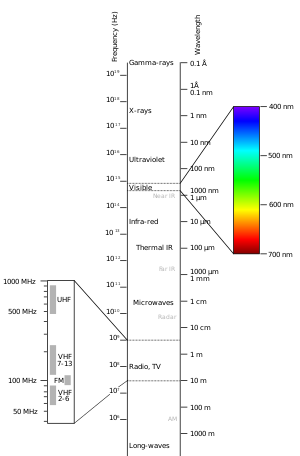
UV- och synlig absorption är en process där en molekyl absorberar ultraviolett eller synligt ljus vilket exciterar elektroner (gör dem energirika). Den absorberade energin driver en elektronisk övergång från ett grundtillstånd till ett exciterat tillstånd. Metoden kallas vanligen UV–vis (UV- och synlig) absorptionsspektroskopi och är en grundläggande teknik inom kemi, biokemi och materialvetenskap för både kvalitativ och kvantitativ analys.
Grundläggande principer
Elektroner i molekyler sitter i olika molekylorbitaler. När energi från ljus matchar energiskillnaden mellan två orbitaler kan en elektron övergå, exempelvis från ett bindande π-orbital till ett antibindande π* (π→π*) eller från ett icke-bindande n-orbital till π* (n→π*). Olika typer av övergångar ger upphov till absorption vid olika våglängder:
- π→π* : vanliga i konjugerade system (alkener, aromater) — ofta starka band i UV/vis.
- n→π* : svagare band, känsliga för lösningsmediets polaritet.
- d–d och charge-transfer : förekommer i övergångsmetallkomplex och ger ofta absorption i synligt område (färg).
Spektral information
- λmax — våglängden för maximal absorption; användbar för identifiering av kromoforer.
- Molar absorptivitet (ε) — ett mått på hur starkt en molekyl absorberar vid en viss våglängd (enhet M−1 cm−1).
- Bands form — breda eller smala band, vibroniska strukturer och skuggor (shoulders) kan ge information om molekylens miljö och struktur.
- Solvens- och pH-effekter kan förskjuta band (bathokromisk eller hypsochromisk förskjutning) eller ändra intensitet (hyperchromic/hypochromic effekter).
Kvantisering — Beer–Lambert lagen
Absorbansen A följer oftast Beer–Lambert lagen: A = ε · c · l, där c är koncentrationen, l är banlängden (cm) och ε molar absorptivitet. Detta gör tekniken lämplig för noggranna koncentrationsbestämningar så länge systemet är linjärt (inga koncentrationsberoende interaktioner eller ljusspridning).
Instrumentuppbyggnad
- Ljus-källa: deuteriumlampor för UV, glödtråd (tungsten) för synligt.
- Monokromator eller filter: selekterar våglängd eller smal bandbredd.
- Provcell (cuvett): kvarts för UV; glas/plast kan användas i synligt område beroende på transmissionskrav.
- Detektor: fotomultiplikator, fotodiod eller diode-array för snabb spektral registrering.
Tillämpningar
- Kvantitativ bestämning av koncentrationer i lösningar (läkemedel, miljöprover, biologiska prover).
- Övervakning av reaktioner och kinetik genom tidsupplösning av absorbansförändringar.
- Kvalitativ identifiering av kromoforer och konjugationens längd (t.ex. färgämnen, pigment).
- Studier av protein- och nukleinsyra-koncentrationer och bindningsinteraktioner.
- Analys av komplexbildning i övergångsmetallkemi (där synligt band kan avslöja ligandfältseffekter).
Praktiska råd och begränsningar
- Använd alltid ett tomt prov (blank) med samma lösningsmedel för att korrigera bakgrundsabsorption.
- Välj lämplig koncentration så att absorbansen ligger i linjärt område (ofta 0,1–1,0 A); för höga värden kräver spädning eller kortare cuvettlängd.
- Undvik ljusspridning från partiklar eller emulsioner — filtrera eller centrifiugera prover om nödvändigt.
- Komplettera med andra tekniker (IR, NMR, MS, fluorescens) när strukturell information krävs utöver elektroniska övergångar.
Sammanfattning
UV–vis absorptionsspektroskopi är en snabb, känslig och lättanvänd metod för att studera elektroniska övergångar i molekyler. Genom att analysera våglängd, intensitet och bandform får man både kvalitativ och kvantitativ information om provets sammansättning, konjugation och miljö. För bästa resultat krävs korrekt provberedning, kalibrering enligt Beer–Lambert och förståelse för vilka övergångstyper som ger upphov till de observerade banden.
Se även tekniken absorptionsspektroskopi för mer allmän bakgrund och metodrelaterade detaljer.