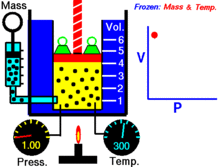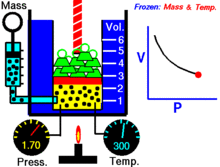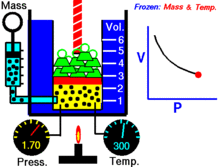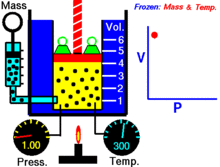
Boyles lag (även kallad Mariottes lag och Boyle–Mariottes lag) är en lag för idealgaser vid konstant temperatur och konstant mängd gas. Den beskriver hur trycket och volymen förhåller sig till varandra vid en isoterm process.
För en fast mängd av en idealgas som hålls vid en fast temperatur är P (tryck) och V (volym) omvänt proportionella.
Formel
I korthet säger lagen att volymen av en given massa gas vid konstant temperatur är omvänt proportionell mot trycket som läggs på gasen. Detta kan uttryckas som
P ∝ 1 V {\displaystyle P\propto {\frac {1}{V}}}
eller
P V = k {\displaystyle PV=k}
där P är gasens tryck, V är gasens volym och k är en konstant (givet antal mol och konstant temperatur). Eftersom konstanten k är samma för två tillstånd av samma gas under isoterm process kan man skriva
P 1 V 1 = P 2 V 2 {\displaystyle P_{1}V_{1}=P_{2}V_{2}}}
Härledning
Boyles lag följer direkt från idealgaslagen PV = nRT. Om mängden gas (n) och temperaturen (T) är konstanta blir nR T också en konstant, vilket ger PV = konstant.
Intuitiv förklaring
Om du minskar volymen i en behållare utan att släppa ut gas så ligger samma antal gaspartiklar i ett mindre utrymme. Partiklarna kolliderar oftare med behållarens väggar, vilket leder till ett högre tryck. Om volymen halveras (vid oförändrad temperatur och mängd) fördubblas trycket.
Exempel
Exempel: En gas har ett tryck på 3 atm och en volym på 5 liter. Om trycket minskas till 2 atm, hur stor blir volymen?
P 1 V 1 = P 2 V 2 {\displaystyle P_{1}V_{1}=P_{2}V_{2}}}
Om vi löser för V2 får vi
V 2 = P 1 V 1 P 2 {\displaystyle V_{2}={\frac {P_{1}V_{1}}}{P_{2}}}}
V 2 = 3 ∗ 5 2 {\displaystyle V_{2}={\frac {3*5}{2}}}}
V 2 = 15 2 {\displaystyle V_{2}={\frac {15}{2}}}}
V 2 = 7.5 {\displaystyle V_{2}=7.5}
∴ Volymen blir 7,5 liter (observera att decimalkomma används i svenska texter: 7,5 L).
Praktiska tillämpningar
- Syringar och sprutor: när kolven trycks in minskar volymen och trycket ökar.
- Däck och däckpumpning: trycket i ett luftfyllt däck förändras med volym och temperatur.
- Laboratorieexperiment och uppgifter i fysik/kemikurser som illustrerar isotermiska processer.
Begränsningar och noggrannhet
Boyles lag gäller för idealgaser under isotermiska förhållanden och när gasens mängd är konstant. Vid höga tryck eller låga temperaturer avviker verkliga gaser från idealbeteendet. För sådana fall används mer avancerade modeller, t.ex. van der Waals ekvation, som tar hänsyn till partiklars volym och attraktiva krafter mellan molekyler.
Historia
Lagen upptäcktes av Robert Boyle 1662 och identifierades oberoende av Edme Mariotte omkring 1679. Därför kallas den ofta både Boyles lag och Mariottes lag.