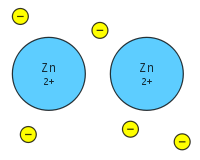
Metallisk bindning innebär att många positiva joner (atomkärnor med sina inre elektroner) är inbäddade i ett delokaliserat "hav" av fria elektroner. Dessa elektroner är inte knutna till en enskild atom utan kan röra sig fritt genom hela kristallgittret. Elektronernas rörlighet fungerar som ett slags bindmedel som håller de positivt laddade jonernas regelbundna ordning samman och ger metaller deras karakteristiska egenskaper.
Varför bildas metallbindning?
Metaller har i allmänhet låg joniseringsenergi, vilket gör att deras valenselektroner lätt kan frigöras från enskilda atomer och bli delokaliserade. Istället för att helt förlora elektroner och bilda joner (som i joniska bindningar) eller att dela elektroner i par (som i kovalenta bindningar), överlappar metallatomernas yttre atomorbitaler och bildar breda energiband. I många fall överlappar valensbandet och ledningsbandet; detta är en förenklad förklaring till varför metaller leder ström.
Egenskaper som följer av metallbindningen
- Elektrisk ledningsförmåga: Eftersom elektronerna kan röra sig fritt leder metaller elektricitet effektivt. Den fria elektronrörelsen möjliggör en snabb förflyttning av laddning och därmed en ström.
- Värmeledningsförmåga: Fria elektroner kan också transportera termisk energi mycket effektivt, vilket gör metaller goda ledare av värme (ledning av värme).
- Glans (lyster): Metaller är ofta blanka (lyster) därför att fria elektroner kan absorbera och återutsända ljus mycket effektivt vid ytan.
- Formbarhet och duktilitet: Metallbindningen är icke-riktad (elektronerna binder inte specifikt mellan bestämda atompar). När ett skjuv-slag förskjuter atomsik gitterbildning kan atomerna glida förbi varandra utan att bindningen bryts, vilket ger metaller formbarhet och duktilitet.
- Styrka och smält-/kokpunkt: Den starka attraktionskraften mellan de positiva jonerna och det negativa elektronhavet ger ofta höga smält- och kokpunkter, och påverkar styrkan. Styrka och smältpunkt varierar dock mycket mellan olika metaller beroende på antal valenselektroner och gitterstruktur.
Fysikalisk förklaring — banden och elektronmolnet
I enklare modeller beskrivs metallbindningen som ett "hav av elektroner". I en modernare beskrivning används bandteori: atomernas diskreta energinivåer breddas till energiband när många atomer kommer nära varandra. I metaller finns delokaliserade elektroner i band som antingen överlappar eller inte är fullständigt fyllda, vilket gör att elektroner kan ta emot och avge energi i små steg och därmed röra sig genom materialet.
Undantag och variationer
Alla metaller uppvisar inte endast metalliska bindningar i alla situationer. Vissa metallföreningar kan uppvisa kovalenta eller joniska karaktär, och metalliska atomer kan under särskilda kemiska förhållanden bilda kovalenta metall–metallbindningar. Ett exempel som nämnts i originaltexten är kvicksilverjoner: Hg2+
2, som kan ingå i andra typer av bindningar. Dessutom finns det icke-metaller som leder elektricitet, till exempel grafit, eftersom grafit har delokaliserade elektroner i plana skikt, och joniska ämnen leder när de är smälta eller lösta eftersom jonerna blir rörliga.
Alloys (legeringar)
En legering är en homogen blandning av två eller flera grundämnen där minst ett är en metall. Legeringar utnyttjar metallbindningens flexibilitet för att förbättra egenskaper som hårdhet, styrka, korrosionsbeständighet eller smältpunkt. Exempel är stål (järn-kol), brons (koppar-tenn) och mässing (koppar-zink). I legeringar kan atomerna sitta i samma gitter (substitutionella legeringar) eller fylla mellanrum i gitterstrukturen (interstitiella legeringar).
Sammanfattning
Metallbindningen — delokaliserade valenselektroner som rör sig fritt bland positiva joner — förklarar många av metallernas typiska egenskaper: hög elektrisk och termisk ledningsförmåga, glans, formbarhet, duktilitet och ofta hög smältpunkt. Styrkan och detaljerna varierar mellan olika metaller och beroende på elektronkonfiguration, kristallstruktur och närvaro av legeringsämnen.