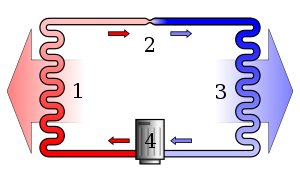
Termodynamikens andra lag säger att när energi övergår från en form till en annan eller när materia rör sig fritt ökar entropin (oordningen) i ett slutet system.
Skillnader i temperatur, tryck och densitet tenderar att jämna ut sig horisontellt efter ett tag. På grund av tyngdkraften jämnar inte densitet och tryck ut sig vertikalt. Densiteten och trycket kommer att vara större på botten än på toppen.
Entropi är ett mått på hur materia och energi sprids överallt där de har tillträde.
Den vanligaste formuleringen av termodynamikens andra lag är i huvudsak Rudolf Clausius:
Med andra ord försöker allting hålla samma temperatur över tiden.
Det finns många uttalanden om den andra lagen som använder olika termer, men som alla betyder samma sak. Ett annat uttalande av Clausius är:
Värme kan inte i sig själv överföras från en kallare till en varmare kropp.
Ett motsvarande uttalande av Lord Kelvin är:
En omvandling vars enda slutresultat är att omvandla värme, som utvinns från en källa med konstant temperatur, till arbete är omöjlig.
Den andra lagen gäller endast för stora system. Den andra lagen handlar om det sannolika beteendet hos ett system där ingen energi eller materia kommer in eller ut. Ju större systemet är, desto mer sannolikt är det att den andra lagen är sann.
Frågor och svar
F: Vad är termodynamikens andra huvudsats?
S: Termodynamikens andra huvudsats säger att när energi övergår från en form till en annan, eller materia rör sig fritt, ökar entropin (oordningen) i ett slutet system.
F: Vad tenderar att jämna ut sig horisontellt över tid?
S: Skillnader i temperatur, tryck och densitet tenderar att jämnas ut horisontellt efter ett tag.
F: Varför utjämnas inte densitet och tryck vertikalt?
S: På grund av gravitationskraften utjämnas inte densitet och tryck vertikalt. Densitet och tryck på botten kommer att vara större än på toppen.
F: Vad är entropi?
S: Entropi är ett mått på hur materia och energi sprids överallt där de finns.
F: Vilken är den vanligaste formuleringen för termodynamikens andra huvudsats?
S: Den vanligaste formuleringen av termodynamikens andra huvudsats beror i huvudsak på Rudolf Clausius: allting försöker hålla samma temperatur över tiden.
F: Vad är ett annat uttalande av Clausius om termodynamikens andra huvudsats?
S: Ett annat uttalande av Clausius är att värme inte i sig kan överföras från en kallare till en varmare kropp.
F: På vilken typ av system är termodynamikens andra huvudsats tillämplig?
S: Termodynamikens andra huvudsats gäller bara för stora system, där ingen energi eller materia kommer in eller ut. Ju större systemet är, desto mer sannolikt är det att den andra huvudsatsen är sann.