Röntgenkristallografi är en experimentell metod för att bestämma en molekyls tredimensionella struktur på atomär nivå. Metoden utnyttjar att elektrontätheten i atomer sprider (böjer) röntgenstrålarna. Genom att mäta hur strålarna diffrakteras får man ett diffraktionsmönster som efter matematisk omräkning kan omvandlas till en bild av elektronmolnet — en så kallad elektrontäthetskarta — och därifrån byggs en atomsmodell av molekylen.
Hur metoden fungerar i praktiken
Grundstegen i röntgenkristallografi är vanligen:
- Odling av en kristall av ämnet. För biologiska makromolekyler (proteiner, nukleinsyror) krävs ofta högkvalitativa, ordnade kristaller.
- Montering av kristallen i en strålgång och exponering för en kontrollerad röntgenstråle. Det finns både laboratoriekällor och kraftfulla synkrotronstrålkällor.
- Inspelning av diffraktionsmönster från olika vinklar. Mönstret består av punkter (reflektioner) med olika intensiteter.
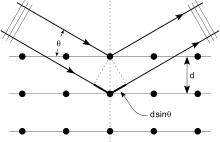
- Tillämpning av Braggs lag och Fouriertransformer för att omvandla diffraktionsdata till en elektrontäthetskarta.
- Modellbygge och finjustering (refinement) av atompositioner för att få en konsekvent struktur som förklarar mätdata. Kvaliteten anges bland annat med upplösning (i ångström, Å) och R-faktor.
Röntgenkristallografi kräver regelbunden ordning i materialet — därför används tekniken främst på kristaller (single-crystal XRD) eller på pulver (powder XRD) när enskilda kristaller inte är tillgängliga. Upplösningen bestämmer hur tydligt man kan se detaljer: låg siffra i Å (t.ex. 1,0 Å) ger hög upplösning medan 3–4 Å ger en mer grov vy av strukturen.
Historia och betydelse
Tekniken utvecklades tidigt genom arbeten av Sir William Bragg (1862–1942) och hans son Sir Lawrence Bragg (1890–1971). De belönades med Nobelpriset i fysik 1915 för sina insatser; Lawrence Bragg är den yngste som fått Nobelpriset i fysik. Lawrence Bragg ledde senare Cavendish Laboratory vid Cambridge University när James D. Watson, Francis Crick, Maurice Wilkins och Rosalind Franklin upptäckte DNA:s struktur i februari 1953 — ett genombrott där röntgendiffraktion av DNA-spjälor spelade en viktig roll.
Tillämpningar
Röntgenkristallografi används inom många områden:
- Strukturkemi: bestämning av små molekylers geometri och bindningslängder.
- Strukturbiologi: bestämning av proteiners och nukleinsyrors tredimensionella strukturer för att förstå funktion och mekanismer.
- Läkemedelsutveckling: strukturstödd design av läkemedel där detaljer om bindningsställen hos målproteiner är avgörande.
- Materialvetenskap och mineralogi: kartläggning av kristallstrukturer i nya material och mineraler.
Begränsningar och moderna förbättringar
Traditionella begränsningar är behovet av välordnade kristaller och risken för strålskador. Påståendet att "Provet förstörs inte under processen" är för enkelt — höga stråldoser kan orsaka kemisk eller strukturell skada, särskilt för känsliga biologiska kristaller. För att minska skador används ofta kylning (kryo-kylning) och kortare exponeringstider. Moderna tekniker som synkrotronljus och frielektronlasrar (XFEL) gör det möjligt att mäta svagare signaler och ibland "läsa ut" strukturen snabbare än skadan uppstår (så kallad serial femtosecond crystallography).
Andra utvecklingar inkluderar bättre detektorer, automatiserad datainsamling och avancerade datoralgoritmer för att tolka svårtolkade mappar, samt metoder för att analysera mycket små kristaller eller mosaik-kristaller.
Tolkning och kvalitet
Efter datainsamling bygger forskaren en atommodell i elektrontäthetskartan och finjusterar den tills beräknade och observerade diffraktionsintensiteter stämmer väl. Kvalitetsmått är bland annat upplösning, R-work/R-free och geometriska parametrar. Uppgifter i PDB (Protein Data Bank) innehåller dessa mått som hjälper användare att bedöma hur mycket strukturdata kan litas på.
Sammanfattning
Röntgenkristallografi är en kraftfull metod för att avgöra molekylers exakta tredimensionella uppbyggnad. Metoden har varit central för många vetenskapliga genombrott och fortsätter utvecklas med nya ljuskällor och beräkningsmetoder. För bästa resultat krävs ofta goda kristaller, omsorg vid datainsamling och modern beräkningsanalys — och uppmärksamhet på strålskador vid känsliga prover.