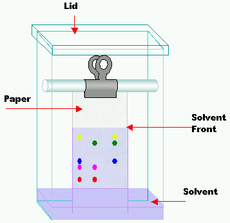
Kromatografi är en metod som använder blandade ämnen som beror på hur snabbt de rör sig genom särskilda medier eller kemiska ämnen. Den består av en stationär fas (ett fast ämne) och en rörlig fas (en vätska eller en gas). Den mobila fasen strömmar genom den stationära fasen. Kromatografi används mycket inom biokemi och analytisk kemi.
Principer
Kromatografisk separation bygger på att olika komponenter i en blandning interagerar olika starkt med den stationära respektive den rörliga fasen. Komponenten som interagerar svagast med den stationära fasen följer med den rörliga fasen snabbare och eluerar först. De viktigaste mekanismerna är:
- Adsorption – ämnen fäster på ytan av den stationära fasen (vanligt i tunnskikts- och kolumnkromatografi).
- Partition – fördelning mellan två flytande faser (t.ex. i vätskekromatografi).
- Jonbyte – separation baserad på laddning (används för joner och polära molekyler).
- Storleksuteslutning (SEC/GPC) – molekyler separeras efter storlek; större molekyler eluerar först.
- Affinitet – selektiv bindning mellan målsubstans och en ligand i den stationära fasen (vanligt inom rening av proteiner).
Vanliga typer av kromatografi
- Papperkromatografi – enkel form för skol- och kvalitativa analyser.
- Tunnskiktskromatografi (TLC) – snabb screening och kontroll av reaktioner.
- Kolumnkromatografi – preparativ separation i labbskala (silica- eller aluminiumbaserad).
- Gaskromatografi (GC) – för flyktiga och termiskt stabila ämnen, ofta kopplat till masspektrometri (GC–MS).
- Högpresterande vätskekromatografi (HPLC/UPLC) – mycket användbar för polaritet, läkemedel, metaboliter och kemisk analys; kan kopplas till detektorer som UV eller MS.
- Jonbyteskromatografi – för separation av syror, baser och salter.
- Affinitetskromatografi – selektiv rening av biomolekyler genom bindning till immobiliserade ligander.
Detektorer och analys
Efter separation måste ämnen oftast detekteras. Vanliga detektorer är:
- UV/Vis – vanlig vid HPLC för aromatiska och konjugerade ämnen.
- Refraktiv index (RI) – generisk men mindre känslig, används för kolhydrater och polymerer.
- Fluorescens – mycket känslig för fluorescerande föreningar.
- Masspektrometri (MS) – ger både känslig kvantifiering och molekylär information (vanligt vid GC–MS och LC–MS).
Användningsområden inom kemi
Kromatografi är central i många analytiska och preparativa tillämpningar:
- Reningsmetoder för syntetiska produkter eller naturliga extrakt.
- Kvantitativ och kvalitativ bestämning av föroreningar, läkemedel och metaboliter.
- Miljöövervakning (t.ex. pesticider, flyktiga organiska föreningar).
- Proteomik och metabolomik inom biokemi och molekylärbiologi.
- Rättsmedicinska analyser, livsmedelskontroll och klinisk diagnostik.
Praktiska överväganden
Vid metodutveckling väljer man lämplig kombination av stationär fas, mobil fas och detektor beroende på provets egenskaper. Några tips:
- Använd provrensning (filtrering, extraktion) för att undvika kolonnförgiftning.
- Optimera flöde, temperatur (särskilt för GC) och gradient (vid HPLC) för bästa separationstid och upplösning.
- Använd interna standarder för kvantitativ analys och kalibreringskurvor för noggrannhet.
- Tänk på kompatibilitet mellan prov och detektor (t.ex. saltsubstanser kan påverka MS).
Fördelar och begränsningar
Fördelar: hög upplösning, bred tillämpbarhet, möjlighet till både analys och preparativ separation, och koppling till känsliga detektorer.
Begränsningar: viss metodutveckling krävs, kostnad för instrument (särskilt HPLC/GC–MS), begränsad kompatibilitet mellan prov och vissa kolonner eller detektorer samt avfalls- och lösningsmedelshantering.
Kort historik
Kromatografins grundidéer utvecklades i början av 1900‑talet; en viktig pionjär var Mikhail Tsvet som använde kolonnkromatografi för separation av växtpigment. Sedan dess har tekniken utvecklats kraftigt och blivit central inom modern kemi och biokemi.
Säkerhet och miljö
Hantera organiska lösningsmedel och gaser enligt laboratoriums rutiner. Minimera avfall genom metodoptimering och välj miljövänligare lösningsmedel när det är möjligt. Följ lokala regler för avfallshantering och emissioner.
Sammanfattningsvis är kromatografi en flexibel och kraftfull grupp av metoder för separation och analys, med många varianter anpassade till olika typer av prover och frågor inom biokemi och analytisk kemi.