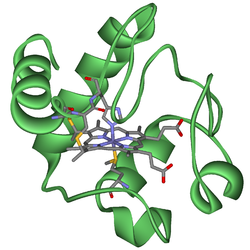
Cytochromer är hemoproteiner (eller proteiner som innehåller hemgrupper) som deltar i biologisk energimetabolism. De bidrar till bildning av ATP genom elektrontransport, där hemgruppens järn växlar mellan reducerad (Fe2+) och oxiderad (Fe3+) form och därigenom överför elektroner mellan redoxcentra.
Monomeriska och komplexbundna former
Cytochromer förekommer både som enskilda (monomera) proteiner, till exempel cytochrom c, och som delar i större enzymkomplex som katalyserar redoxreaktioner. Exempel på sådana komplex är mitokondriens komplex III (cytochrom bc1) och komplex IV (cytochrom c‑oxidas), samt bakteriers och växters motsvarigheter såsom cytochrome b6f i fotosyntetiska membraner.
Struktur och indelning
- Typer av hem: Cytochromer skiljer sig åt beroende på vilken typ av hemgrupp de innehåller (t.ex. heme a, heme b, heme c). Dessa hemgrupper bestämmer ofta proteinetens elektroniska egenskaper och redoxpotential.
- Typer efter bokstav: Vanliga grupper kallas cytochrom a, b och c. Cytochrom c är ett litet, lösligt protein i mitokondriens intermembranrum som fungerar som elektronbärare mellan komplex III och IV. I kontrast är cytochrom b och a ofta membranbundna delar av större komplex.
- Kovalent bindning: I c‑typen binds hemegruppen kovalent till proteinet via en Cys‑X‑X‑Cys‑motif, medan a‑ och b‑typerna vanligen håller hemgruppen icke‑kovalent.
Funktion i elektrontransportkedjan
I mitokondrier och hos många bakterier transporterar cytochromer elektroner längs en kedja av redoxproteiner från elektrondonatorer (t.ex. NADH eller FADH2) till slutliga acceptorer (hos aeroba organismer är det oftast syre). Denna elektrontransport är kopplad till protonpumpning över ett membran, vilket skapar en protongradient (protonmotorkraft) som driver ATP-syntas att syntetisera ATP.
En förenklad elektronström i mitokondriens respirationskedja: complex I/II → ubiquinon → complex III (cytochrom bc1) → cytochrom c (löslig bärare) → complex IV (cytochrom c‑oxidas) → O2. I fotosyntes fungerar motsvarande steg via plastokinon och cytochrom b6f.
Biokemiska egenskaper och analys
- Redoxreaktioner: Hemgruppen utför redoxreaktionerna — det är här oxidationstalen ändras och elektroner överförs. Genom att järnet i hem går mellan Fe2+ och Fe3+ kan cytochromer ta emot och avge elektroner i snabba cykler.
- Spektroskopiska egenskaper: Reducerade och oxiderade former av cytochromer har karakteristiska absorptionsband i det synliga spektrumet. Detta utnyttjas experimentellt för att följa reduktionsgrad och kinetik i elektrontransporten.
- Enzymatiskt sammanhang: Cytochromer ingår ofta i komplex som inte bara överför elektroner utan också kopplar denna överföring till protontranslokation eller andra kemiska steg.
Biologisk och klinisk betydelse
Förutom deras centrala roll i energiproduktion har vissa cytochromer viktiga sidofunktioner. Ett välkänt exempel är cytochrom c som, vid skada på mitokondriens yttre membran, kan frisättas till cytosolen och där initiera apoptos genom att hjälpa till att bilda apoptosomen och aktivera kaspaser.
Störningar i cytochrom‑funktion eller i uppbyggnaden av deras komplex kan leda till mitokondriella sjukdomar och nedsatt cellulär energiomsättning. Cytochromer används också i laboratoriet för att mäta andningsaktivitet (t.ex. cytochrom c‑oxidas‑aktivitet) och som indikatorer på oxidativ stress eller mitokondriell skada.
Sammanfattning: Cytochromer är hemproteiner vars hemgrupp möjliggör växling mellan oxiderade och reducerade tillstånd, och därigenom effektiv elektrontransport. Genom att vara antingen lösliga bärare eller delar av stora membranbundna komplex spelar de en avgörande roll för cellens förmåga att omvandla redoxenergi till ATP.