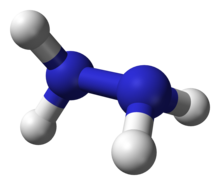
Hydrazin är en kemisk förening med den kemiska formeln N2 H4. Molekylen kan beskrivas som H2N–NH2 och består av kväve- och vätejoner i mening av att den innehåller kväve- och väteatomer; i själva molekylen är bindningarna kovalenta och ämnet finns inte som fria joner under normala förhållanden. Varje väte har formellt oxidationstalet +1 medan kvävenas sammanlagda oxidationstal är -4 (i genomsnitt -2 per kväveatom).
Fysiska och kemiska egenskaper
- Utseende: färglös, oljig vätska (ren hydrazin kan vara starkt frätande och luktande).
- Smält- och kokpunkt: smältpunkt nära 2 °C och kokpunkt omkring 114 °C (ungefärliga värden för ren hydrazin).
- Löslighet: blandbar med vatten och många polära lösningsmedel.
- Kemi: starkt reduktionsmedel som reagerar kraftigt med oxidationsmedel; bildar lätt derivat som hydrazoner och används i reduktioner (t.ex. Wolff–Kishner-reduktionen av karbonylföreningar).
- Struktur: två kväveatomer bundna med enkelbindning (N–N) och ett lone pair på varje kväve, vilket ger en pyramidal geometri kring kvävene.
Framställning
- Historiskt vanliga processer är Raschig-processen (t.ex. från ammoniak och hypoklorit) och modernare katalytiska processer med väteperoxid och ammoniak. Olika industriella metoder används beroende på önskad renhet och miljökrav.
- Hydrazin förekommer också i formen hydrazinhydrat (vattenlösning), som är vanlig i industriell hantering och applikationer.
Användningsområden
- Raket- och flygindustrin: används som drivmedel (monopropellant eller i bipropellant-system) eftersom den sönderdelas exoterma till kvävgas och andra lätta gaser och därigenom ger högt drivtryck.
- Vattenbehandling: fungerar som syreavskiljare (oxygen scavenger) i pannor och vattenkretsar för att minska korrosion.
- Kemisk industri och organisk syntes: utgångsämne för tillverkning av plaster, läkemedel, jordbruksprodukter och för syntessteg som involverar hydrazoner och reducerande reaktioner.
- Laboratorieanvändning: reagens i olika synteser och analysmetoder.
Säkerhet och miljö
- Toxicitet: hydrazin är giftigt vid inandning, hudkontakt och intag. Långtids- och upprepad exponering kan ge allvarliga hälsokonsekvenser; ämnet misstänks vara cancerframkallande i vissa bedömningar.
- Brand- och explosionsrisk: lättantändligt och bildar explosiva blandningar med luft; reagerar våldsamt med många oxidationsmedel.
- Hantering: hanteras bäst i slutna system med personlig skyddsutrustning (handskar, skyddsglasögon, andningsskydd vid risk för ångor) och god ventilation. Förvaring i väl tillslutna behållare, skyddat mot värme och oxidationsmedel.
- Miljö: är giftigt för vattenlevande organismer och bör inte släppas ut i naturen; spill skall hanteras enligt lokala föreskrifter för farligt avfall.
Kort kemisk sammanfattning
Hydrazin är ett mångsidigt men farligt reducerande ämne med formeln N2 H4. Dess reaktivitet gör det användbart i industriella och kemiska processer, men dess toxicitet och brandrisk kräver strikta säkerhetsrutiner vid produktion, lagring och användning.