Osmos (/ɒzˈmoʊ.sɪs/) är den spontana rörelsen av lösningsmedelsmolekyler (vanligtvis vatten) genom ett membran som är selektivt genomsläppligt, från en region med högre andel lösningsmedel (lägre halt lösta ämnen) till en region med lägre andel lösningsmedel (högre halt lösta ämnen). Rörelsen sker utan yttre kraft och beror på molekylernas slumpmässiga termiska rörelse. Eftersom membranet tillåter passage av lösningsmedlet men inte av vissa lösta partiklar, leder diffunden till att koncentrationerna på båda sidor efterhand jämnas ut.
Varför uppstår osmos?
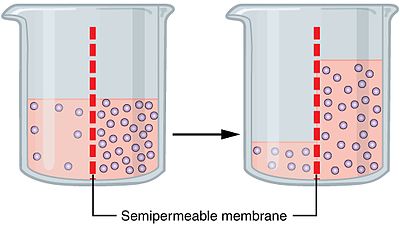
Osmos uppstår eftersom ett semipermeabelt membran skiljer två vätskeområden så att endast lösningsmedlet (t.ex. vatten) kan passera fritt. Eftersom lösningsmedelsmolekyler hela tiden rör sig statistiskt, blir det en nettotransport mot den sida som innehåller fler lösta partiklar. Man kan tänka så här: vatten "söker" jämvikt genom att späda ut den sidan som har högst koncentration av lösta ämnen.
Osmotiskt tryck
Det osmotiska trycket är det yttre tryck som måste tillämpas på lösningen med högre koncentration av lösta ämnen för att stoppa nettoflödet av lösningsmedel genom membranet. Osmotiskt tryck beräknas i många fall med van ’t Hoffs lag för idealiska lösningar:
Π = i M R T
där Π är det osmotiska trycket, i är van ’t Hoffs faktor (antal lösta partiklar som bildas per formelenhet), M är molar koncentration, R är gaskonstanten och T temperaturen i Kelvin. I praktiken påverkas osmoticitet också av jonstyrka, joninteraktioner och membranets egenskaper.
I det ursprungliga avsnittet nämns att osmos kan göras effektiv — det innebär att man utnyttjar osmos för teknik eller separation, exempelvis för att avskilja vatten från lösta ämnen.
Toniska förhållanden: isotont, hypertoniskt och hypotoniskt
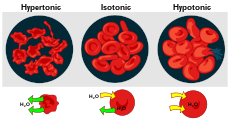
- Isoton lösning: samma osmotiska tryck som cellens inre — ingen nettoförändring i cellvolym.
- Hyperton lösning: högre koncentration av lösta ämnen utanför cellen än innanför — cellen förlorar vatten och krymper (plasmolys i växtceller).
- Hypoton lösning: lägre koncentration av lösta ämnen utanför cellen än innanför — cellen tar upp vatten och kan svälla eller till och med spricka (lysis) om trycket blir för högt.
Osmos i biologiska system
Osmos är centralt för vattenbalans i alla levande celler eftersom biologiska membran oftast är halvgenomsläppliga. Generellt är membranen relativt ogenomträngliga för stora och laddade molekyler (joner, proteiner, polysackarider) men genomsläppliga för små opolära eller oladdade molekyler som syre och koldioxid. Permeabiliteten beror på löslighet, laddning, kemiska egenskaper och storlek hos den lösta substansen.
Vattenmolekyler kan passera genom fosfolipiddubbelskiktet, men i många celler underlättas transporten via kanalproteiner kallade aquaporiner, som ger snabb och kontrollerad vattenpassage. Osmos är därmed det huvudsakliga sättet för vatten att komma in i och ut ur cellerna och spelar en avgörande roll för cellens turgor och funktion.
Skillnad mellan växter och djur
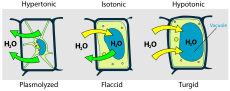
Växtceller har en styv cellvägg som motverkar överdriven utvidgning när vatten tas upp; det inre trycket kallas turgor och är viktigt för att hålla upp växtens vävnader. Om växtceller hamnar i en hyperton lösning krymper protoplasten och lossnar från cellväggen (plasmolys).
Djurceller saknar cellvägg och är därför mer känsliga för osmotiska förändringar. Ett exempel med klinisk relevans är att ge intravenösa vätskor som är isotona (t.ex. 0,9 % NaCl) för att undvika att blodkroppar krymper eller sväller.
Osmoreglering och fysiologiska exempel
Organismer kontrollerar sin vatten- och jonbalans genom osmoreglering. Människans njurar reglerar blodets osmolaritet genom att koncentrera eller späda urin, styrt av hormoner som ADH (antidiuretiskt hormon). Fiskar och andra vattenlevande djur har särskilda mekanismer för att anpassa sig till söt- eller saltvattenmiljöer.
Mätning, demonstration och tekniska tillämpningar
Osmos kan demonstreras enkelt med en dialys- eller cellulosamembran i ett U-rör eller med plastpåsar (dialyspåsar) i olika salthalter. Osmotiskt tryck kan mätas med manometrar eller beräknas från lösningens sammansättning.
Tekniska tillämpningar inkluderar omvänd osmos (RO) för vattenrening, där man applicerar ett yttre tryck större än det osmotiska trycket för att tvinga vatten genom ett membran och på så sätt avskilja lösta salter och föroreningar. Osmos används också i processindustri, livsmedelsindustri och läkemedelstillverkning.
Sammanfattning
Osmos är en fundamental fysikalisk process där lösningsmedel rör sig genom ett semipermeabelt membran från en region med relativt högre andel lösningsmedel till en region med lägre andel lösningsmedel. Processen styr vattenbalans i celler, genererar osmotiskt tryck och har både biologiska och tekniska tillämpningar. Förståelsen av osmos är viktig för områden som fysiologi, medicin, växtbiologi och vattenrening.