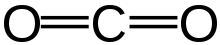Översikt
Koldioxid, kemiskt betecknad CO2, är en enkel kemisk förening som i vanliga omständigheter förekommer som en färglös gas. I atmosfären, i vattenlösningar och i olika industriella processer spelar den flera roller som både är naturliga och människoskapat. För grundläggande information om ämnet och dess klassificering, se kemisk förening och dess tillstånd som gas vid vanlig rumstemperatur.
Kemiska och fysiska egenskaper
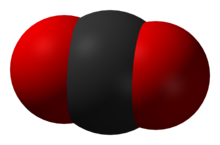
Molekylen består av en central kolatom bunden till två syreatomer i en linjär konfiguration. Vid normala temperaturer och tryck är CO2 en gas, men under högt tryck eller kyla kan den bli vätska och vid ännu lägre temperatur sublimerar den till fast form, ofta kallad torr-is. Den löser sig i vatten och bildar svag kolsyra, vilket påverkar vattenkemi och levande organismer.
Koldioxid i naturen och kolcykeln
Koldioxid ingår i jordens kolcykel som rör utbyte mellan atmosfär, biosfär, hydrosfär och geosfär. Växter och vissa mikroorganismer tar upp CO2 vid fotosyntes och omvandlar den till biomassa, en process som ofta beskrivs i material om växter och fotosyntes. Genom att använda koldioxid för att bygga näring bidrar växter till att binda kol i mark och växtmaterial. Samtidigt frigörs koldioxid vid respirationsprocesser, nedbrytning och naturliga eller mänskliga förbränningshändelser, inklusive eld och bränder.
Biologisk betydelse
Koldioxid är en viktig substrat för alla fotosyntetiska organismer och ett centralt element i energiflödet i ekosystem. Växternas förmåga att dra ner CO2 påverkar primärproduktionen i ekosystemen. Mikroorganismer i jord och hav bryter ner organiskt material och återför CO2 till atmosfären, vilket gör mekanismer för upptag och utsläpp avgörande för kolbalansen.
Klimatpåverkan och växthuseffekt
CO2 räknas som en betydande växthusgas eftersom den absorberar och återutstrålar värmeenergi i atmosfären. Ökade halter förstärker den naturliga växthuseffekten och bidrar till klimatförändringar och skiftande väder. Diskussioner om jordens framtid och klimatpolitik berör hela vår planet och jorden som system, där begrepp som klimatförändringar och global uppvärmning ofta används för att beskriva observerade trender vid jordens yta.
Havsförsurning
När koldioxid löser sig i havsvatten bildas kolsyra, vilket sänker pH och förändrar kemin i marina miljöer. Detta kan påverka organismer som skaldjur och koraller genom att göra kalkbildning svårare och rubba näringskedjor. Effekterna är komplexa och varierar regionalt beroende på temperatur, salthalt och lokala ekosystem.
Mätning, gränsvärden och hälsorisker
Koldioxidhalter i atmosfären mäts kontinuerligt av forskningsstationer och i lokala sensornät. I slutna utrymmen kan höga koncentrationer orsaka obehag eller hälsoproblem; därför rekommenderas god ventilation i bostäder, skolor och arbetsplatser för att hålla nivåer inom säkra gränser. Vid förbränningsolyckor eller dålig ventilation kan risker öka och kräva snabba åtgärder.
Användningar och industriell betydelse
- Industriellt används CO2 bland annat i kolsyrning av drycker, i kylningsprocesser som torr-is och i vissa tillverkningsprocesser.
- I vissa kemiska processer används den som råmaterial eller inert gas för att förhindra oönskad oxidation.
- Tekniker för koldioxidavskiljning, -lagring och återanvändning utvecklas som en del av strategier för att minska nettoutsläpp.
Åtgärder och policy
För att hantera koldioxidens roll i klimatförändringarna kombineras minskade utsläpp genom energieffektivisering och omställning till förnybar energi med naturbaserade lösningar som återbeskogning och tekniska metoder som koldioxidinfångning och -lagring. Val av åtgärder styrs av både vetenskapliga bedömningar och politiska beslut och är föremål för kontinuerlig utvärdering.
Historia
De tidiga studierna av gasers egenskaper inkluderade arbete av 1700-talets kemister. Den skotske kemisten Joseph Black var en av dem som beskrev förändringar i luftarter under kemiska reaktioner på 1750-talet, vilket lade grunden för senare förståelse av koldioxidens natur och betydelse.
Sammanfattningsvis är koldioxid en mångfacetterad molekyl med betydelse för kemi, biologi, industri och klimat. Fördjupningar finns via länkar till ämnen som föreningar, gasers fysik, växternas ekologi, fotosyntes och historiska studier av forskare som Joseph Black (1750-tal), samt centrala begrepp inom klimatforskning och klimatpolitik.