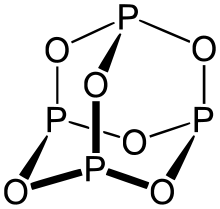
Fosfor(III)oxid, även känd som fosfortrioxid, är en kemisk förening med den empiriska formeln P2O3 och den molekylära formeln P4O6. I denna förening är fosfor i oxidationstillstånd +3. Historiskt och i vissa förenklade formuleringar anges den som innehållande fosfor- och oxidjoner, men P4O6 är i praktiken en kovalent molekylisk förening snarare än ett rent joniskt salt.
Struktur
P4O6 har en kovalent, cage-liknande struktur som kan beskrivas som en tetraeder av fyra fosforatomer där de sex kanterna är "bryggade" av sex syreatomer. Varje syreatom länkar två fosforatomer (P–O–P) och varje fosfor är därför trigonalt bunden till tre syreatomer och bär en elektronpar (lone pair). Denna geometri förklarar fosfors +3-oxidationstillstånd och molekylens relativt långa P–O-bindningar jämfört med enkla P–O‑jonbindningar.
Egenskaper
- Utseende: färglös till svagt gulfärgad kristallin fast substans under standardförhållanden.
- Molekylvikt: cirka 219,9 g·mol−1 för P4O6.
- Löslighet: reagerar med vatten (hydrolyserar) och löses i vissa organiska lösningsmedel; hydrolys är snabbare i varm eller surt medium.
- Kemisk natur: fungerar som anhydrid till fosfor(III)-syra (fosforonsyra, H3PO3) och uppvisar reduktionsbeteende i många reaktioner.
Framställning
P4O6 framställs i laboratorium genom kontrollerad oxidation av vit fosfor (P4) i begränsad mängd syrgas. Vid fullständig oxidation bildas istället P4O10 (fosfor(V)oxid). Genom att noggrant reglera mängden tillgängligt syre kan man erhålla den tredimensionella P4O6-föreningen.
Reaktivitet och viktiga reaktioner
- Hydrolys: P4O6 hydrolyserar i vatten och bildar fosfor(III)-syra enligt reaktionen:
P4O6 + 6 H2O → 4 H3PO3. - Oxidation: i luft oxideras P4O6 gradvis till P4O10.
- Reduktiva egenskaper: kan verka som reduktionsmedel och reagera med starka oxidationsmedel eller halogener.
Användning
P4O6 har begränsad industriell användning men förekommer som reagens i organisk och oorganisk syntes samt i forskning kring fosfor-kemiska system. Det är också betydelsefullt som konceptuellt exempel på icke‑jonisk fosfor‑oxid och som anhydrid till H3PO3.
Säkerhet och hantering
- Toxicitet: ämnet är giftigt och irriterande för luftvägarna; ångor eller damm kan ge hosta, andningsbesvär och allvarlig irritation.
- Reaktivitet: reagerar med fukt och oxiderar i luft; bör hållas borta från starka oxiderande ämnen.
- Försiktighetsåtgärder: hantera i dragskåp, använd lämplig skyddsutrustning (handskar, skyddsglasögon, andningsskydd vid behov) och förvara i tättslutande, luftfria behållare under inert gas eller torr atmosfär.
Sammanfattning: Fosfor(III)oxid (P4O6) är en kovalent, molekylär fosfor-oxid med fosfor i oxidationstillstånd +3. Den är anhydrid till fosfor(III)-syra, hydrolyserar i vatten och oxideras i luft till P4O10. På grund av dess toxicitet och reaktivitet används den främst i kontrollerade laboratoriemiljöer.