p53 (eller tp53) är en gen som är viktig för många livsformer, inklusive människor. Den kodar för ett protein som motverkar cancer. Den har kallats "genomets väktare".
P53-genen är den mest frekvent muterade genen (>50 %) i mänsklig cancer. Dess proteinprodukt binder till DNA och reglerar genuttrycket för att förhindra mutationer i genomet.
p53-proteinet (TP53) finns i låga nivåer i mänskliga embryonala stamceller (hESC). Detta gör att den viktigaste celldelningen kan ske snabbt.
Funktioner och verkningsmekanismer
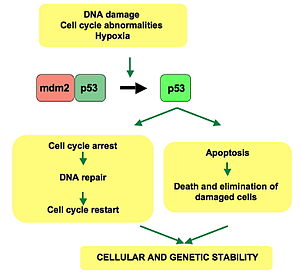
p53 är en transkriptionsfaktor som reagerar på olika typer av cellulär stress, till exempel DNA‑skada, oxidativ stress, hypoxi och onkogen aktivering. När p53 aktiveras påverkar proteinet uttrycket av ett flertal gener som leder till olika cellulära utfall. De viktigaste funktionerna är:
- Cellcykelstopp: p53 kan inducera uttryck av proteiner (t.ex. p21) som bromsar cellcykeln för att ge tid för DNA‑reparation.
- Apoptos (programmerad celldöd): Om skadan är allvarlig kan p53 utlösa apoptos för att ta bort farliga celler.
- Senescens: p53 kan inducera en permanent tillväxthämning (cellsenescens) som hindrar fortsatt delning av potentiellt tumörbildande celler.
- DNA‑reparation: p53 reglerar gener som är inblandade i reparationsprocesser och bibehåller genomintegritet.
- Metabolism och autofagi: p53 påverkar också cellens ämnesomsättning och autofagi, vilket kan påverka cellöverlevnad vid stress.
Under normala förhållanden hålls p53-nivåerna låga genom negativ reglering, framför allt av E3‑ubiquitinligasen MDM2 som märker p53 för nedbrytning. Vid DNA‑skada aktiveras kinaser som ATM och ATR som fosforylerar p53 (och/eller MDM2), vilket stabiliserar p53 och låter det verka i kärnan.
Mutationer och roll i cancer
Mutationer i TP53 är mycket vanliga i mänskliga tumörer och kan ha flera konsekvenser:
- Förlust av funktion: Mutationer kan helt eliminera p53:s förmåga att binda DNA och reglera genuttryck, vilket leder till minskad kontroll över cellcykel och ökad genomisk instabilitet.
- Dominant‑negativa effekter: Vissa muterade p53‑proteiner kan störa funktionen hos kvarvarande normalt p53.
- Gain‑of‑function: Vissa mutationer ger p53 nya egenskaper som aktivt kan främja tumörutveckling, invasivitet eller resistens mot behandling.
Utöver somatikiska mutationer finns ärftliga TP53‑mutationer som orsakar Li‑Fraumeni‑syndrom, en ärftlig sjukdom som ger mycket hög risk för flera olika tidiga cancerformer.
Klinisk betydelse och forskning
p53 har stor klinisk betydelse på flera sätt:
- Diagnostik och prognos: TP53‑status används inom forskning och ibland kliniskt som markör för prognos och behandlingsval i vissa cancerformer.
- Terapeutiska strategier: Flera strategier utvecklas för att återställa p53‑funktionen eller utnyttja dess väg för behandling, bland annat MDM2‑hämmare (som blockerar nedbrytning av vilt‑typ p53), små molekyler som kan återaktivera vissa mutanta p53‑former (t.ex. PRIMA‑1/ APR‑246), samt genterapier och immunterapier i experimentella studier.
- Läkemedelsresistens: Mutationer i TP53 kan påverka tumörers känslighet för kemoterapi och strålning eftersom många behandlingar förlitar sig på p53‑medierad celldöd.
Forskning på p53 bedrivs i många modellorganismer (från jäst och maskar till möss) och inkluderar studier av p53‑familjen, som även omfattar proteinerna p63 och p73 som har överlappande och egna funktioner i utveckling och tumörsuppresssion.
p53 i utveckling och stamceller
I embryonala stamceller och andra snabbt delande celler är p53‑nivåerna ofta låga för att möjliggöra snabb proliferation. Samtidigt finns mekanismer för att snabbt aktivera p53 vid allvarlig skada för att skydda organismens integritet. Balansen mellan snabb delning och genomskydd är viktig under utveckling och i vävnadsstamceller.
Sammanfattningsvis är p53 en central tumörsuppressorgen som via många mekanismer bevarar genomintegriteten. Dess ofta förekommande mutationer i cancer gör den till ett viktigt fokus för grundforskning och klinisk utveckling av nya behandlingsmetoder.