Översikt
pH är ett mått på hur surt eller basiskt en vattenlösning är. Ett lägre pH innebär högre surhet, ett högre pH innebär mer basisk (alkalisk) karaktär och värdet 7 brukar kallas neutralt vid vanlig temperatur. Begreppet används brett inom kemi, biologi, miljövetenskap och teknik för att beskriva egenskaper hos ämnen i lösning och deras reaktivitet.
Definition och formler
Den vanliga formella definitionen i undervisning och praktiska tillämpningar är
pH = −log10[H+],
där [H+] avser koncentrationen av vätejoner i mol per liter. Denna förenklade form används ofta i laboratorier och fältmätningar. Mer korrekt anges pH i termer av jonaktivitet:
pH = −log10 aH+,
där aH+ betecknar vätejonens aktivitet, vilket tar hänsyn till interaktioner i lösningen som gör att frijonernas effekt skiljer sig från deras nominella koncentration. I många vanliga lösningar ger båda uttrycken nästan samma värde.
Mätmetoder
pH bestäms på flera sätt, beroende på önskad noggrannhet och omständigheter:
- pH-meter: elektronisk mätning med elektrod som ger direkt numeriskt värde och är standard i laboratorier.
- pH-indikatorer: färgämnen som förändras över ett pH-intervall och används för snabb visuell bedömning.
- pH-papper: enkelt, bärbart papper med flera färgområden för approximativa mätningar.
Samtida rapporter och manualer beskriver kalibrering och temperaturkompensation för att få tillförlitliga resultat.
Historik och terminologi
Begreppet infördes av kemisten S. P. L. Sørensen omkring Sørensen 1909. Bokstaven P kommer från tyska ordet potenz (makt eller potens) och H betecknar vätejonen, ofta skriven som H+. Formeln och skalan etablerades snabbt som en praktisk och intuitiv metod att uttrycka stora variationer i vätejonkoncentration på en logaritmisk skala.
Användning, exempel och betydelse
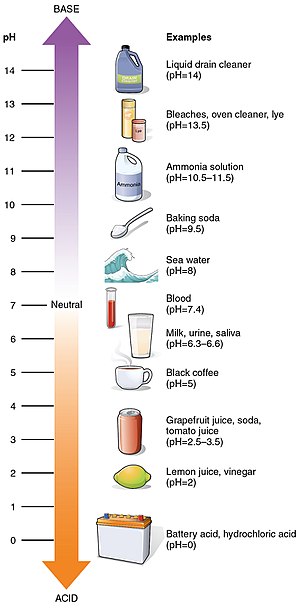
pH påverkar kemiska jämvikter, löslighet, biologiska processer och materialkorrosion. Exempel på vanligt förekommande pH-värden:
- Maginnehåll i människans mage är mycket surt (lågt pH, ofta omkring 1–2) vilket underlättar nedbrytning av föda.
- Blodets pH är nära neutralt men lätt basiskt (vanligtvis omkring 7,4), vilket är viktigt för enzymfunktion och homeostas.
- Rent vatten vid standardförhållanden har pH omkring 7, medan avloppsvatten kan vara surare eller mer basiskt beroende på föroreningar.
I miljöövervakning används pH för att följa försurning i mark och vatten, medan industriprocesser ofta kräver strikt kontroll av pH för produktkvalitet.
Ytterligare fakta och avvikelser
Skalan 0–14 är ett praktiskt spann för många vardagliga lösningar, men under extrema förhållanden kan pH vara mindre än 0 eller större än 14. pH är temperaturberoende och buffertsystem kan motverka snabba förändringar genom att binda eller frigöra vätejoner. Begreppet skiljer också mellan syra/bas enligt olika teorier: i Brønsted–Lowry-termer definieras syror som protondonatorer och baser som protonacceptorer; i en vattenlösning motsvarar höga [OH−] en basisk lösning.
Vidare läsning
För fördjupning i begrepp, mätteknik och praktiska riktlinjer se följande källor: syror, alkalier, lösningar, beräkning, mol, liter, molaritet, och allmänt material om syror och baser i läroböcker.
Se även vidare information om experimentell praxis och säkerhet när du arbetar med starkt sura eller basiska lösningar.
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}](https://www.alegsaonline.com/image/093977a79b6a17e02db4699475930e48c05d6468.svg)
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}](https://www.alegsaonline.com/image/7a631c4037415f3d4483a6cb07e69858b64890fc.svg)