Aktiveringsenergin för en kemisk reaktion är den minsta energi som behövs för att reaktionen ska ske. Den har vanligtvis symbolen Ea och mäts i kilojoule per mol (kJ·mol⁻¹), men kan också anges i joule per mol (J·mol⁻¹). Den kan ses som en barriär mellan reagenserna och produkterna i en reaktion. Aktiveringsenergin är skillnaden i energi mellan övergångstillståndet och startreagenserna.
Definition och enhet
Aktiveringsenergi (Ea) är den energikälla som krävs för att bilda det högenergiska övergångstillståndet från reaktanterna. Enheten uttrycks vanligen i kJ·mol⁻¹ eller J·mol⁻¹. Numeriskt anger Ea hur stor andel av kollisionerna mellan molekyler som har tillräcklig energi för att leda till en reaktion vid en given temperatur.
Hur aktiveringsenergin påverkar reaktionshastigheten
Reaktionshastigheten är mycket känslig för Ea. Ju högre aktiveringsenergi, desto färre kollisioner når övergångstillståndet och desto långsammare blir reaktionen vid samma temperatur. Ökad temperatur gör att fler partiklar har tillräcklig energi, vilket kraftigt ökar reaktionshastigheten.
Arrhenius-ekvationen och bestämning av Ea
Relationen mellan hastighetskonstanten k och aktiveringsenergin beskrivs av Arrhenius-ekvationen:
k = A · exp(−Ea / (R·T))
där A är frekvensfaktorn (ett mått på hur ofta lämpliga kollisioner sker), R är gaskonstanten (8,314 J·mol⁻¹·K⁻¹) och T är temperaturen i Kelvin. Genom att mäta k vid flera temperaturer och plotta ln(k) mot 1/T fås en rät linje med lutningen −Ea/R, vilket används för att bestämma Ea experimentellt.
Katalysatorers roll
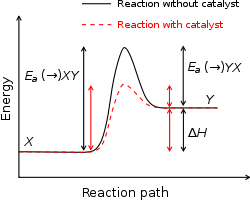
Katalysatorer ökar reaktionshastigheten genom att erbjuda en alternativ reaktionsväg med lägre aktiveringsenergi. De förändrar alltså Ea (sänker den) men påverkar inte reaktionens totala energiförändring (ΔH) eller jämviktsläget, endast hur snabbt jämvikt nås.
Fram- och bakåtreaktioner samt energidiagram
En reaktion har vanligen två aktiveringsenergier: Ea,f för framåtriktningen och Ea,b för bakåtreaktionen. Förhållandet mellan dem och reaktionens entalpiförändring ΔH är:
ΔH = Ea,f − Ea,b
På ett potentiellt energidiagram visas reaktanternas energi, övergångstillståndets topp och produkternas energi; höjden från reaktanterna till toppen är Ea.
Typiska värden och exempel
- Många organiska och oorganiska reaktioner har Ea i spannet från några tiotals till flera hundra kJ·mol⁻¹.
- Enzymatiska reaktioner (biologiska katalysatorer) kan visa mycket lägre effektiva aktiveringsenergier, vilket möjliggör snabba reaktioner vid kroppstemperatur.
Praktiska anmärkningar
- Ett lägre Ea ger snabbare reaktion vid samma temperatur, men jämviktsläget bestäms av termodynamiken (ΔG, ΔH) och påverkas inte av katalysatorer.
- Ea kan uppskattas teoretiskt med beräkningar av övergångstillstånd eller bestämmas experimentellt med Arrhenius-plot.
- Vid mycket höga temperaturer kan andra faktorer (t.ex. sidoreaktioner eller sönderfall) påverka observerade hastigheter, så tolkning kräver försiktighet.
Sammanfattningsvis är aktiveringsenergin ett centralt begrepp för att förstå hur och varför kemiska reaktioner går snabbare eller långsammare under olika förhållanden, och hur katalysatorer effektivt kan påverka reaktionshastigheter utan att ändra slutligen uppnådd jämvikt.