Kemisk kinetik, även kallad reaktionskinetik, är att studera hur snabbt kemiska reaktioner går. Detta innefattar studier av hur olika förhållanden, t.ex. temperatur, tryck eller lösningsmedel, påverkar reaktionshastigheten. Kemisk kinetik kan också användas för att ta reda på reaktionsmekanismer och övergångstillstånd.
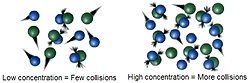
Den grundläggande idén om kemisk kinetik kallas kollisionsteori. Enligt denna teori måste molekylerna träffa varandra för att en reaktion ska kunna ske. För att öka reaktionshastigheten måste man därför öka antalet träffar. Detta kan göras på många olika sätt.
Med hjälp av experiment är det möjligt att beräkna reaktionshastigheter som ger upphov till hastighetslagar och hastighetskonstanter. En hastighetslag är ett matematiskt uttryck som gör det möjligt att beräkna hastigheten för en reaktion givet koncentrationen av reagenserna.
Vad menas med reaktionshastighet?
Reaktionshastigheten är förändringen i koncentration av en reaktant eller produkt per tidsenhet. Den kan anges som en genomsnittlig hastighet över ett tidsintervall eller som en momentan (differentiell) hastighet i ett givet ögonblick. För en allmän reaktion A + B → produkter skrivs en vanlig differential form av hastighetslagen som:
rate = k [A]^m [B]^n
Här är k hastighetskonstanten och m och n är reaktionsordningar som bestäms experimentellt. Den totala reaktionsordningen är m + n.
Olika faktorer som påverkar reaktionshastigheten
- Temperatur: Ökad temperatur ger fler och mer energirika kollisioner. Detta beskrivs ofta med Arrhenius-ekvationen k = A · exp(−Ea/RT), där Ea är aktiveringsenergin, R gaskonstanten och A frekvensfaktorn.
- Koncentration: Högre koncentration av reaktanter ger fler kollisioner per tidsenhet och ofta högre hastighet (beroende på ordning).
- Katalysatorer: Katalysatorer sänker aktiveringsenergin och ändrar reaktionsmekanismen utan att själva förbrukas, vilket ökar hastigheten.
- Tryck och fas: För gasreaktioner påverkar höjt tryck ofta hastigheten genom effektivt högre koncentration. I heterogena system påverkar yta/volym och adsorption till ytan reaktionshastigheten.
- Lösningsmedel och jonstyrka: Polära lösningsmedel, växelverkan mellan joner och lösningsmedlets egenskaper kan modifiera aktiveringsbarriärer och därmed hastigheten.
- Diffusionsbegränsning: I vissa fall är reaktionen begränsad av hur snabbt reaktanter kan diffundera ihop, t.ex. i mycket viskösa medier eller på ytor.
Reaktionsordning och integrerade hastighetslagar
Beroende på experimentella data kan en reaktions hastighetslag vara noll-, första- eller andra ordning (eller högre). Några vanliga integrerade former:
- Nollte ordningen: [A] = [A]0 − k t (hastigheten är konstant)
- Första ordningen: ln[A] = ln[A]0 − k t (ger en linjär graf av ln[A] vs t)
- Andra ordningen (en komponent): 1/[A] = 1/[A]0 + k t
Första ordningens halveringstid ges av t1/2 = ln(2)/k och är oberoende av startkoncentrationen — en ofta använd egenskap för att diagnostisera första ordningen kinetik.
Reaktionsmekanismer och elementarsteg
Hastighetslagen speglar ofta inte direkt stökiometrin i overallreaktionen utan de elementära stegen i mekanismen. En mekanism består av en serie elementarsteg (molekularitet: unimolekylär, bimolekylär osv.) som leder från reaktanter till produkter via mellanprodukter och ett övergångstillstånd (aktiverat komplex).
Vanliga metoder för att förenkla analys av mekanismer:
- Steady-state-approximation: Antar att koncentrationen av reaktiva mellanprodukter är konstant (bildningshastighet ≈ förbrukningshastighet).
- Pre-equilibrium-approximation: Antar att vissa tidiga steg uppnår jämvikt snabbare än de följande långsammare stegen.
Experimentella metoder för att bestämma kinetik
Några vanliga tekniker för att mäta reaktionshastigheter:
- Spektrofotometri: Mäter absorbansändringar över tid för färgade ämnen eller bildade produkter.
- Konduktimetri och manometri: Används när jonstyrka eller gasvolym förändras.
- Calorimetri: Mäter värmeändringar vid reaktioner.
- Stopped-flow och flash-fotolys: För mycket snabba reaktioner (millisekunder till mikrosekunder).
- Isotop- och kinetiska isotop-effekter: Byta ut atomtyper (t.ex. H → D) visar vilken bindning som bryts i hastighetsbestämmande steg.
Temperaturberoende och aktiveringsenergi
Genom att mäta hastighetskonstanter vid flera temperaturer kan man bestämma aktiveringsenergin Ea genom att plotta ln k mot 1/T (Arrhenius-plot). Lutningen är −Ea/R. Detta ger insikter i energibarriärer och om en katalysator eller annan förändring påverkar mekanismen.
Praktiska begrepp och tillämpningar
- Pseudo-förstagrad: Om en reaktant hålls i stor överhängande överskott blir hastighetslaget effektivt första ordning i den andra reaktanten, vilket förenklar analysen.
- Kinetik i industri och miljö: Kinetisk kunskap används för att designa reaktorer, optimera katalysatorer, uppskatta förvarstid för läkemedel och förutsäga nedbrytning i miljön.
- Beräkningar och modellering: Modern kinetik kombinerar experiment med teoretiska metoder som övergångstillståndsteori och datorberäkningar för att kartlägga mekanismer och energiprofil.
Sammanfattningsvis ger kemisk kinetik verktygen för att förstå hur snabbt reaktioner sker, varför hastigheten ändras under olika villkor och vilka steg som styr reaktionshastigheten — information som är grundläggande både inom forskning och i praktiska tillämpningar.