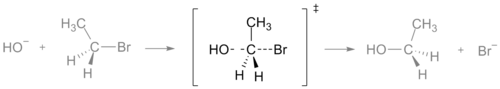Översikt
Inom kemi beskriver begreppet kemisk reaktion hur ämnen omvandlas till andra ämnen. Mitt i denna omvandling finns ofta ett övergångstillstånd — den punkt på reaktionsvägen där det potentiella energidiagrammet når sin högsta nivå. För att nå detta tillstånd måste reaktanterna tillföra den så kallade aktiveringsenergin. Om kolliderande molekyler har tillräcklig energi kan de passera denna barriär, vilket leder till att gamla bindningar bryts och nya börjar bildas. Övergångstillståndets symbol är ofta markerad med en dubbel dolk, ‡, i vetenskapliga diagram.
Karakteristika
Övergångstillståndet är inte en isolerbar art; det är ett konfigurationsläge på den potentiella energiytan snarare än en stabil molekyl. Det existerar bara under mycket korta tidsperioder och har vanligtvis hög energi jämfört med både reaktanter och produkter. Viktiga egenskaper är att vissa bindningar är delvis brutna medan andra är delvis bildade, och att geometrin ofta är en mix mellan utgångs- och slutstruktur. I kemisk teori används begreppet "aktiverat komplex" synonymt i vissa sammanhang, men praktisk distinktion görs ofta mot intermediärer.
Skillnad från intermediär
Det är viktigt att skilja mellan ett övergångstillstånd och en intermediär. En intermediär återfinns i en lokal energiminimum på energiytan och kan ibland isoleras eller i alla fall ha en bestämd livslängd som överstiger övergångstillståndets. Övergångstillståndet ligger däremot i en energimaksimum och kan inte fångas upp som en separat kemisk art. Båda befinner sig mellan utgångsämnen och produkter men har olika experimentella och teoretiska konsekvenser.
Studier och metoder
Direkt observation av övergångstillstånd är svår, men moderna tekniker ger indirekt eller beräkningsmässig insikt. Experimentellt används snabb spektroskopi och pumpprover-uppsättningar för att följa extremt snabba processer, medan masspektrometri och kryokonditionering kan indikera kortlivade intermediära steg. Teoretiskt beräknas övergångstillstånd genom kvantkemiska metoder och analys av den potentiella energiytan. Sådana beräkningar är centrala för att förstå reaktionsmekanismer och förutsäga aktiveringsenergier inom kemisk kinetik.
Användning och betydelse
Kännedom om övergångstillståndets geometri och energi är praktiskt viktig: det hjälper kemister att designa katalysatorer som sänker aktiveringsenergin och därmed ökar reaktionshastigheten. Inom organisk syntes, enzymologi och materialvetenskap används övergångstillståndsteori för att optimera selektivitet och utbyte. I tillämpad forskning leder förståelsen av dessa toppar ofta till effektivare processer, lägre energiförbrukning och nya syntetiska strategier.
Sammanfattning och noteringar
- Övergångstillståndet är en högenergipunkt på reaktionsvägen, markerad med ‡.
- Det är kortlivat och kan inte isoleras som en stabil molekyl.
- Intermediärer är däremot stabilare och ligger i energiminima.
- Både experimentella och beräkningsmetoder används för att karaktärisera övergångstillstånd och därigenom förstå hur och varför reaktioner sker.
För vidare läsning om relaterade begrepp, se artiklar om kemisk reaktion, aktiveringsenergi och reaktionsmekanismer, eller använd de övriga ämneslänkarna för djupare studier: molekyler, bindningar, intermediärer, kemisk kinetik.