Översikt
En kemisk reaktion är en process där en eller flera ämnen omvandlas till andra ämnen genom att kemiska bindningar bryts och nya bildas. Reaktanterna i början av processen blir produkter i slutet, samtidigt som atomerna omfördelas men inte försvinner — massan bevaras. Exempel på vardagliga reaktioner är järn som rostar, mat som bryns vid stekning och koldioxid som frigörs när ättika reagerar med bakpulver.
Egenskaper och drivkrafter
Kemiska reaktioner påverkas av temperatur, koncentration, tryck (särskilt för gaser), yta och närvaro av katalysatorer. Temperatur kan öka reaktionshastigheten genom att fler partiklar når den energi som krävs för att reagera. En katalysator sänker aktiveringsenergin och ändrar normalt inte jämviktsläget, bara hur snabbt det nås. Energiflödet är viktigt: exoterma reaktioner avger värme och endotermiska tar upp värme.
Vanliga reaktionstyper
- Redoxreaktioner: elektronöverföringar som vid rostning eller cellandning.
- Syrabasreaktioner: protonöverföringar mellan syra och bas.
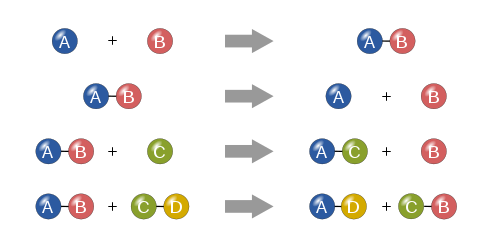
- Bildnings- och sönderdelningsreaktioner: syntes av större molekyler eller sönderdelning i mindre komponenter.
- Fällningsreaktioner: bildning av olösliga salter i lösning.
- Elektrokemiska reaktioner: kemiska förändringar kopplade till elektrisk ström, vilket sker i batterier.
Tillämpningar och betydelse
Kemiska reaktioner ligger till grund för många tekniker och processer inom industri, medicin och miljövetenskap. De används för att framställa plaster, läkemedel, gödselmedel och bränslen, och styrs i laboratorier för att skapa nya material. I biologiska system sker ständigt kemiska reaktioner som möjliggör metabolism, fotosyntes och nervsignalering. I energisammanhang är förmågan att kontrollera reaktionshastighet och värmeutbyte central för både säkerhet och effektivitet.
Skillnad mot kärnreaktioner
Kemiska reaktioner involverar atomernas elektroner och förändrar hur atomerna binds till varandra. Kärnreaktioner påverkar däremot atomkärnans protoner och neutroner och förändrar ibland grundämnets identitet. På grund av detta skiljer sig deras energiskalor, risker och tillämpningar — kärnreaktioner kan frigöra mycket större energimängder och kräver andra säkerhetsåtgärder än vanliga kemiska processer.
Noterbara begrepp och exempel
För att sätta begreppen i sammanhang: rostning är en långsam oxidation där järn reagerar med syre och fukt, medan reaktionen mellan ättika och bakpulver är snabb och bildar koldioxidgas. Förbränning är en snabb, ofta exo- term process som frigör värme och ljus. Batterier bygger på elektrokemiska reaktioner där kemisk energi omvandlas till elektrisk. Många industriella processer använder katalysatorer för att göra reaktioner mer effektiva och mindre energikrävande.
Vidare läsning och resurser
- Allmänt om kemiska reaktioner
- Järn och dess kemi
- Syrets roll i reaktioner
- Rost och korrosion
- Ättikans kemi
- Bakpulver och dess funktion
- Natriumacetat — exempelprodukt
- Koldioxid i kemiska reaktioner
- Elektrokemi översikt
- Batterier och lagring
- Temperaturens betydelse
- Trä och förbränning
- Luftens komponenter
- Energi i kemiska reaktioner
- Exoterma reaktioner förklarade
- Endoterma processer
- Kärnreaktioner — skillnader
- Elektroner och bindningar
- Protoner i atomkärnan
- Neutronernas roll
- Atomkärnan och dess struktur
Denna text ger en grundläggande orientering om kemiska reaktioner. För djupare studier finns mer detaljerade källor om kinetik, termodynamik och reaktionsmekanismer som behandlar matematiska modeller och experimentella metoder.