Inom kvantmekaniken, en gren av fysiken, är Bohrs atommodell en tidig kvantiserad modell av atomen som föreslogs av Niels Bohr. Modellen används främst för att beskriva väteatomens energinivåer och är särskilt framgångsrik för att förklara vätgasens emissionsspektrum.
Grundläggande antaganden
- Elektronen rör sig i cirkulära banor runt kärnan utan att kontinuerligt avge strålning när den befinner sig i en stationär bana.
- Endast vissa diskreta banor är tillåtna: elektronens rörelsemängdsmoment är kvantiserat enligt m v r = n h / 2π, där n är ett positivt heltal (huvudkvanttalet), m elektronens massa, v hastigheten, r radien och h Plancks konstant.
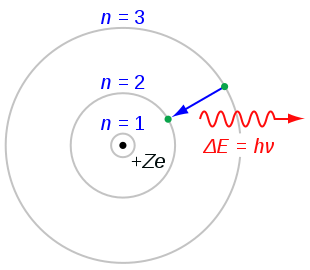
- Övergångar mellan dessa tillåtna banor sker kvantiskt: när en elektron hoppar från en bana med energi E_i till en bana med energi E_f avges eller upptas en foton med energin ΔE = E_i − E_f = hν.
Energier och spektrum
Ur Bohrs antaganden följer att energinivåerna för väte (och väte-liknande, enkel-kärniga joner) ges av
E_n = −13,6 eV / n² (n = 1, 2, 3, ...),
vilket ger diskreta linjer i emissions- och absorptionsspektrumet. Våglängderna för övergångar mellan nivåer n_1 och n_2 kan beskrivas med Rydbergs formel:
1/λ = R (1/n_1² − 1/n_2²),
där R är Rydbergs konstant, R ≈ 1,097·10^7 m⁻¹. Bohrs modell förklarar bland annat Balmer-serien i vätgasspektrumet och ger korrekta värden för de observerade spektrallinjerna i många fall.
Begränsningar och vidareutveckling
- Bohrs modell fungerar mycket väl för väte och väte-liknande joner, men den beskriver inte korrekt fler-elektronssystem där elektron-elektroninteraktioner blir viktiga.
- Modellen tar inte hänsyn till elektronspin, relativistiska effekter eller finstruktur och kan därför inte förklara små förskjutningar av spektrallinjer (t.ex. Zeeman- och Stark-effekter i detalj).
- Som en vidareutveckling införde Arnold Sommerfeld elliptiska banor och relativistiska korrektioner för att förklara finstrukturdelningar, men den fullständiga och mer generella förklaringen kom med Schrödingers vågmekanik och Heisenbergs matrisformulering.
Betydelse
Trots sina begränsningar var Bohrs atommodell ett viktigt steg i utvecklingen av modern kvantteori. Den introducerade idén om kvantiserade energinivåer och gav första förklaringen till atomers spektrallinjer i ett enkelt, intuitivt ramverk. Modellen illustrerar också Bohrs korrespondensprincip: för stora kvanttalsvärden går kvantmekaniken över i klassisk mekanik.