Översikt
Plancks konstant, betecknad h, är en grundläggande konstant i fysiken som anger proportionen mellan en fotons energi och dess frekvens via relationen E = h·ν. Den fungerar som kvantans aktionskvanta och sätter skalan för kvantisering i många fysikaliska sammanhang. Konstanten är universell och oberoende av tid och plats i universum.
Definition och värde
I det internationella SI-systemet har Plancks konstant sedan omdefinitionen av SI-enheter 2019 ett exakt fastställt värde: h = 6,62607015×10^-34 J·s. Detta exakta värde uttrycks och kommenteras ofta som det exakta värdet i metrologiska sammanhang. Värdet används både i teoretiska formler och i praktisk realisering av enheter.
Enheter och dimensioner
Plancks konstant har dimensionen verkan (eller action) och kan uttryckas som energi multiplicerad med tid eller som rörelsemängd multiplicerad med avstånd. I SI-enheter anges den i joule-sekunder (J·s), men motsvarande enhetskombinationer förekommer i litteraturen, till exempel N·m·s eller kg·m²·s⁻¹. Dimensionernas roll diskuteras ofta i samband med dimensionell analys och grundläggande enhetsdefinitioner.
Matematiska samband
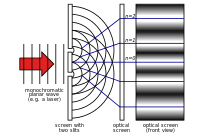
Plancks konstant förekommer i flera centrala samband i kvantfysiken. För en foton gäller E = h·ν, där ν betecknar frekvens och en enskild ljuskvant ofta kallas foton. Sambandet mellan rörelsemängd p och våglängd λ är p = h/λ, vilket är grundläggande för våg-partikeldualiteten. Den reducerade Planckkonstanten ħ = h/(2π) används i Schrödinger-ekvationen och i osäkerhetsrelationen Δx·Δp ≥ ħ/2.
Historik och betydelse
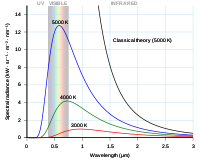
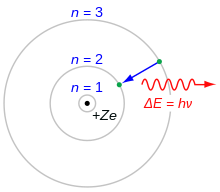
Konstanten är uppkallad efter fysikern Max Planck, som i slutet av 1800-talet och vid sekelskiftet 1900 introducerade idén om kvantisering när han analyserade svartkroppsstrålning. Plancks arbete utgjorde en avgörande startpunkt för kvantmekanikens utveckling. Sedan dess har h varit centralt i beskrivningen av mikroskopiska processer och i förståelsen av fenomen som fotoelektrisk effekt och atomspektrum.
Tillämpningar och betydelse i modern fysik
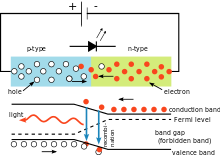
Utöver grundläggande teoretiska uttryck används Plancks konstant i praktiska beräkningar och tekniska tillämpningar. Den är relevant för spektralanalys, kvantiserade energinivåer i atomer och molekyler, samt för beräkningar inom kondensmateriafysik och kvantelektronik. I metrologi spelar h en direkt roll i realiseringen av massanheten via experiment som Kibblevågen, där kilogram kopplas till ett exakt värde på Plancks konstant.
Plancks enheter
Genom att kombinera h med andra fundamentala konstanter kan man definiera Plancks naturliga enheter, som Plancks längd och Plancks tid, vilka beskriver skalor där effekter av både kvantmekanik och gravitation blir jämförbara. Exempelvis diskuteras Plancks längd och Plancks tid i samband med försök att formulera teorier om kvantgravitation.
Begrepp och praktiska noteringar
- Plancks konstant relaterar energi (energi) och frekvens (frekvens) i ett enkelt, linjärt samband.
- Det finns två vanliga beteckningar: h (Plancks konstant) och ħ (h-streck eller "h-bar", den reducerade konstanten).
- Konstanten är universell och oberoende av materialegenskaper eller experimentell plats.
- Enhetssammanhangen förklaras i kontexten av SI-enheter och modern metrologi.
Fördjupning och läsning
För vidare läsning rekommenderas introduktioner till kvantmekanik och metrologi, historiska översikter över Plancks arbete samt tekniska texter om praktisk realisering av SI. Ytterligare diskussioner om dimensioner och enhetsdefinitioner finns under dimensioner och i publikationer om SI-enheter. Grundläggande begrepp såsom vågor, rörelsemängd och avstånd är ofta involverade i tillämpningar där h förekommer.
Sammanfattningsvis är Plancks konstant ett centralt tal i modern fysik som binder samman flera nyckelkoncept: foton-egenskaper, kvantiserade energinivåer och fundamentala enheter. Den exakta fastställningen av dess värde spelar en viktig roll i hur vi definierar och realiserar grundläggande mätetal i dagens vetenskap.








![Illustrationen är hämtad från Newtons originalbrev till Royal Society (1 januari 1671 [juliansk kalender]). S står för solljus. Ljuset mellan planerna BC och DE är i färg. Dessa färger kombineras på nytt för att bilda solljuset på planet GH.](https://www.alegsaonline.com/image/NewtonDualPrismExperiment.jpg)







![{\displaystyle h={\frac {\mu _{0}\pi }{12c^{3}}}{[{q_{0}}{[0.9163a_{0}]}^{2}]^{2}}{f_{1r}}^{5}\cdot {s}=6.63\times 10^{-34}J\cdot s}](https://www.alegsaonline.com/image/4c47db8d0ec87cc985fc3b80db4214489e87a164.svg)










