cykloaddition är en kemisk reaktion mellan reaktanter med dubbelbindningar som ersätts av en ringstruktur. Det är en percyklisk kemisk reaktion där "två eller flera omättade molekyler (eller delar av samma molekyl) kombineras med bildandet av ett cykliskt addukt där det sker en nettominskning av bindningsmultipliciteten". Som sådan är en cykloaddition en cykliseringsreaktion: det bildas en ny ring av atomer och ofta nya enkelbindningar på platser där det tidigare funnits pi-bindningar.
Mekanism och allmänna regler
Cykloadditioner är ofta concerted (sammanhängande) pericykliska processer där elektronfördelningen ändras genom ett cykliskt övergångstillstånd. Reaktionernas möjligheter styrs av orbitalsymmetri enligt Woodward–Hoffmann-reglerna. I praktiken innebär detta att vissa kombinationer är termiskt tillåtna och andra tillåtna först under fotokemiska förutsättningar, beroende på om överlappningen av pi-orbitaler kan ske suprafaciellt eller antarafaciellt.
Notation och vanliga typer
Cykloadditioner betecknas ofta som [m + n], där m och n är antal atomer som bidrar med pi-elektroner till den nya ringen. Vanliga exempel:
- [4 + 2] — Diels-Alder-reaktionen, där en konjugerad diene (4 pi-elektroner) reagerar med en dienofil (2 pi-elektroner) för att bilda en sexring.
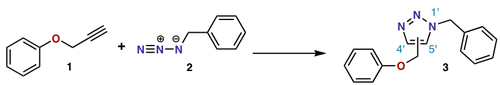
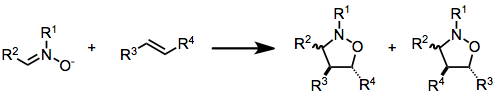
- [3 + 2] — 1,3-dipolarcykloaddition, där en 1,3-dipol adderar till en dubbelbindning (exempel: azid + alkin i vissa varianter).
- [2 + 2] — ofta fotokemiskt tillåtna cykloadditioner som ger fyra-ringar; termiska [2+2]-reaktioner är vanligtvis symmetribundet och ofta förbjudna i ett suprafacialt, concerted förlopp.
- Cheletropiska reaktioner — en specialtyp där båda nya bindningarna formas till samma atom (t.ex. addition av SO2 till en dubbelbindning i vissa fall).
Stereokemi och selektivitet
Cykloadditioner är ofta stereospecifika: substituenternas relativa konfiguration i reaktanterna bestämmer stereokemin i produkten. Diels–Alder-reaktioner visar till exempel vanligtvis retention av dubbelbindningarnas stereokemi och kan ge endo/exo-selektivitet. Endo-preferensen för många Diels–Alder-reaktioner förklaras med sekundära orbitalinteraktioner mellan diene och dienofil, vilket ofta leder till hög stereokontroll.
Orbitalinteraktioner och katalys
Reaktionshastighet och selectivitet beror ofta på HOMO–LUMO-interaktioner. I en typisk Diels–Alder är diene-HOMOen och dienofil-LUMOen viktiga; elektronfattiga dienofiler (med EWG) sänker LUMO-energin och påskyndar reaktionen. Lewis-syror används ofta som katalysatorer för att aktivera dienofiler och öka både hastighet och stereoselektivitet.
Undantag och stegvisa mekanismer
Trots att många cykloadditioner är concerted, kan vissa ske via stegvisa mekanismer med radikal- eller jonlika intermediärer, särskilt under kraftiga fotokemiska eller termiska förhållanden eller med starkt polariserade reaktanter. Sådana vägval kan påverka stereokemi och regiokemi.
Tillämpningar
- Syntes av cykliska system i naturliga produkter och läkemedel — Diels–Alder-reaktionen är ett standardverktyg i totalsyntes.
- Polymerkemisk användning — vissa cykloadditioner utnyttjas i kopplings- och tvärbindningsreaktioner.
- Click-kemi — moderna [3+2]-cycloadditioner, exempelvis koppling mellan azider och alkynes (CuAAC), används flitigt för biokonjugering och materialvetenskap då de är högeffektiva och selektiva.
- Retrosyntetiska strategier — retro-Diels–Alder-reaktioner används för att bryta ringar i kontrollerade sammanhang och i analytiska tillämpningar (t.ex. masspektrometri).
Sammanfattning
Cykloaddition är en viktig klass av pericykliska reaktioner som omvandlar omättade system till ringar enligt väl definierade orbitalregler. De är mångsidiga i syntetisk kemi tack vare god stereokontroll, möjlighet till katalys och ett brett utbud av typer ([4+2], [3+2], [2+2] med flera). För att designa och förstå cykloadditioner är kunskap om orbitalsymmetri, HOMO–LUMO-skillnader och eventuella katalytiska effekter centrala faktorer.
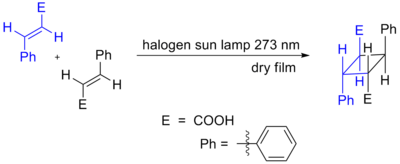
.png)
![Intermolecular Formal [3+3] Cycloaddition Reaction](https://www.alegsaonline.com/image/600px-3+3-cycloaddition.svg.png)