Ädelgaserna är en grupp grundämnen som alla är gaser. Alla dessa grundämnen ingår i grupp 18 i det periodiska systemet. De är alla monoatomära, vilket innebär att varje molekyl består av en enda atom. De reagerar nästan aldrig med andra grundämnen. Detta beror på att de har ett fullständigt yttre elektronskal med 8 elektroner. Det finns sex ädelgaser:
Alla dessa gaser finns i luften. De utgör ungefär 0,96 % av atmosfären. Ädelgasföreningar kan bildas av ädelgaser.
När ädelgaserna används i kalla katodrör för att producera ljus har de olika färger. Eftersom radon är radioaktivt används det vanligtvis inte för belysning. Här är bilder på hur de andra ser ut:
· 
Helium
· 
Neon
· 
Argon
· 
Krypton
· 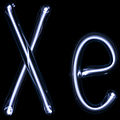
Xenon
Ununoctium (grundämne 118) är förmodligen nästa ädelgas efter radon eftersom det är nästa ruta i samma grupp. Den har dock en halveringstid på 0,89 ms, varefter den sönderfaller till ununhexium (element 116). Detta innebär att dess användning förmodligen är begränsad.
Ädelgaserna upptäcktes av Lord Rayleigh och Sir William Ramsay. Rayleigh fick Nobelpriset i fysik 1904 för sitt arbete med ädelgaser. Ramsay fick Nobelpriset i kemi 1904 för sitt arbete med ädelgaser.
Egenskaper
Elektronkonfiguration: Helium skiljer sig något från de andra eftersom det har det fulla yttre skalet med 2 elektroner (1s2). De övriga ädelgaserna har den så kallade oktettregeln uppfylld (ns2 np6). Detta ger dem mycket låg kemisk reaktivitet.
Fysikaliska egenskaper: Alla är lukt- och färglösa gaser vid standardtryck och -temperatur. Kok- och smältpunkter varierar kraftigt — helium har det lägsta kokpunkten av alla ämnen och blir flytande först vid mycket låga temperaturer (används i kryoteknik). Generellt blir atomradien och polariserbarheten större nedåt i gruppen, vilket gör de tyngre ädelgaserna mer benägna att bilda föreningar än de lättare.
Förekomst i atmosfären
Ädelgaser finns i jordens atmosfär i olika mängder. Argon är vanligast och står för ungefär 0,93 % av luften. Om man summerar bidraget från alla ädelgaser blir det cirka 0,96 %, vilket stämmer väl med siffran ovan. Neon och krypton finns i mycket mindre mängder; helium är relativt ovanligt i atmosfären eftersom det lätt kan undkomma jordens gravitation. Radon är extremt sällsynt i luften eftersom det är radioaktivt och sönderfaller snabbt.
Föreningar och reaktivitet
Trots deras rykte som "inert" kan vissa ädelgaser bilda kemiska föreningar under rätt förhållanden. Reaktiviteten ökar nedåt i gruppen:
- Xenon bildar flera stabila föreningar, till exempel xenonfluorider (XeF2, XeF4, XeF6) och oxidfluorider (XeO3, XeO4 under speciella förhållanden).
- Krypton kan bilda vissa föreningar, exempelvis KrF2.
- Argon och neon är mycket svårare att få att reagera; endast mycket kortlivade och experimentella föreningar eller exciterade komplex har observerats under särskilda laboratorieförhållanden.
- Helium är det minst reaktiva och bildar i praktiken inga stabila kemiska föreningar under normala förhållanden.
Användningar
Ädelgaserna har många tekniska och industriella användningsområden tack vare sina unika egenskaper:
- Helium: Kylning av supraledande magneter (t.ex. i MRI-apparater), gas i ballonger och väderballonger, läckdetektion och som skyddsgas vid vissa svetsprocesser. Helium används också inom kryogenik.
- Neon: Används främst i reklamskyltar ("neonskyltar") och i vissa lysrör för att ge rödorange färg.
- Argon: Vanlig som skyddsgas vid svetsning, i glödlampor och i fetthaltiga processer där man vill undvika oxidation. Argon används också inom metallurgi och analysinstrument.
- Krypton: Används i vissa typer av belysning och i fotografisk utrustning; kryptonfluoridlampor och speciella blixtlampor använder också krypton.
- Xenon: Används i autonoma strålkastare, kraftfulla blixtlampor och inom medicinsk anestesi (i vissa fall). Xenon används även i jonmotorer för rymdfarkoster.
- Radon: På grund av sin radioaktivitet har radon få praktiska nyttor; det är framför allt en hälsorisk inomhus och används ibland i geologisk dateringsforskning och i mycket kontrollerade medicinska sammanhang historiskt, men användningen är i praktiken begränsad på grund av riskerna.
Säkerhet
Ädelgaser är kemiskt ofarliga i den meningen att de inte reagerar med vävnad, men de kan utgöra en kvävningsrisk i slutna utrymmen om de tränger undan syre (särskilt helium, argon och xenon i koncentrerade mängder). Radon är ett undantag: det är radioaktivt och en känd orsak till lungcancer vid långvarig exponering i dåligt ventilerade byggnader. Hantering av radioaktiva gaser kräver särskilda säkerhetsrutiner.
Upptäckt och historik
Flera forskare bidrog till ädelgasernas upptäckt. Lord Rayleigh upptäckte argon när han jämförde densiteten hos kväve från luft med kväve från kemiska föreningar och fann en skillnad – en ny gas fanns i luften. Sir William Ramsay isolerade och identifierade sedan flera andra ädelgaser från luften. Helium observerades först i solens spektrum (av forskare som Janssen och Lockyer) innan det senare påvisades på jorden. Rayleigh fick Nobelpriset i fysik 1904 och Ramsay Nobelpriset i kemi 1904 för sina arbeten med gaser och upptäckter av nya element.
Om element 118
Ununoctium (nu officiellt namn: oganesson, Og) är det syntetiska grundämne som ligger i samma ruta som ädelgaserna. Det produceras i mycket små mängder i kärnreaktorer eller partikelacceleratorer och har extremt kort halveringstid (orden av millisekunder), vilket gör praktiska användningar osannolika. Den korta halveringstiden på cirka 0,89 ms gör att det sönderfaller mycket snabbt till tyngre sönderfallsprodukter.
Sammanfattningsvis är ädelgaserna en unik och viktig grupp i det periodiska systemet: de ger skyddande inert atmosfär i många industriella processer, har speciella användningsområden tack vare sina fysikaliska egenskaper och visar intressanta kemiska beteenden, framför allt för de tyngre medlemmarna i gruppen.