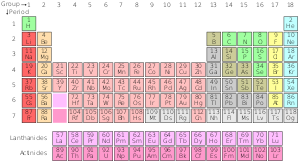
Det periodiska systemet för kemiska grundämnen är en förteckning över kända kemiska grundämnen. I tabellen placeras grundämnena i den ordning de har sina atomnummer och börjar med det lägsta atomnumret, väte. Atomnumret för ett grundämne är detsamma som antalet protoner i just den atomkärnan. I det periodiska systemet är grundämnena indelade i perioder och grupper. En rad av grundämnen över hela tabellen kallas för en period. Varje period har ett nummer, från 1 till 8. Period 1 innehåller endast två grundämnen: väte och helium. Period 2 och period 3 har båda åtta grundämnen. Andra perioder är längre. Elementen i en period har på varandra följande atomnummer.
Perioder
En period är en horisontell rad i tabellen. När man går från vänster till höger över en period ökar atomnumret med ett steg i taget och elektronerna läggs i samma energinivå (samma skal). Detta ger flera viktiga mönster:
- Elektronkonfigurationen ändras systematiskt och påverkar kemiskt beteende.
- Atommassor och atomradier förändras ofta gradvis över perioden.
- Reaktivitet och typ av bindningar (jonisk vs. kovalent) varierar från metalliskt till icke‑metalliskt.
Grupper och gruppnummer
En kolumn av element i tabellen kallas en grupp. Det finns 18 grupper i det vanliga periodiska systemet. Varje grupp har ett nummer: från 1 till 18. Elementen i en grupp har elektroner som är ordnade på liknande sätt, enligt antalet valenselektroner, vilket ger dem liknande kemiska egenskaper (de beter sig på liknande sätt). Till exempel kallas grupp 18 för ädelgaserna eftersom de alla är gaser och inte kombineras med andra atomer.
Det finns två system för gruppnummer, ett med arabiska siffror (1, 2, 3) och ett med romerska siffror (I, II, III). De romerska siffrorna användes under större delen av 1900-talet. År 1990 beslutade Internationella unionen för ren och tillämpad kemi (IUPAC) att använda det nya systemet med arabiska siffror för att ersätta de två gamla gruppsystemen med romerska siffror.
Block och elektronkonfiguration
Tabellen delas också in i block — s-, p-, d- och f-block — beroende på vilken typ av orbital som fylls med den yttersta elektronen. Dessa block förklarar många kemiska egenskaper:
- s‑block: grupperna 1–2 (inklusive väte och helium). Har 1–2 valenselektroner.
- p‑block: grupperna 13–18. Innehåller många icke‑metaller och ädelgaser.
- d‑block: övergångsmetallerna (grupperna 3–12). Karaktäriseras av delokaliserade d‑elektroner.
- f‑block: lantanider och aktinider, ofta separerade längst ner av tabellen.
Lantanider, aktinider och syntetiska element
Längst ner i många tabeller finns lantaniderna och aktiniderna — två rader som omfattar de f‑blockselementen. Många aktinider är radioaktiva. Utöver naturligt förekommande grundämnen finns även syntetiska element som tillverkats i laboratorier; dessa har ofta mycket kort halveringstid.
Periodiska trender
Det periodiska systemet visar flera tydliga trender som hjälper kemister att förutsäga egenskaper:
- Atomradie: ökar nedåt i en grupp och minskar åt höger över en period.
- Ioneringsenergi: energin som krävs för att ta bort en elektron — ökar åt höger och minskar nedåt.
- Elektronegativitet: ett mått på förmågan att dra till sig elektroner i en kemisk bindning — generellt större åt höger och överst i tabellen.
- Reaktivitet: varierar beroende på grupp — alkalimetaller (grupp 1) är mycket reaktiva, ädelgaser (grupp 18) är mycket lite reaktiva.
Metaller, metalloider och icke‑metaller
Det periodiska systemet har använts av kemister för att observera mönster och samband mellan grundämnen. Det finns tre huvudgrupper i det periodiska systemet: metaller, metalloider och icke-metaller. Elementen längst ner och längst till vänster i tabellen är till exempel de mest metalliska, och elementen längst upp till höger är de minst metalliska. (Cesium är t.ex. mycket mer metalliskt än helium). Metaller är ofta glänsande, leder värme och elektricitet väl och bildar positiva joner. Icke‑metaller bildar oftare negativa joner eller delar elektroner i kovalenta bindningar. Metalloider har egenskaper mellan dessa två och används ofta i halvledarteknik.
Historia och Mendelejev
Det periodiska systemet uppfanns av den ryske kemisten Dmitry Ivanovich Mendeleyev (1834-1907). Till hans ära har grundämne 101 uppkallats efter honom, mendelevium. Mendelejev sorterade grundämnena efter atomvikt och förutsåg att det skulle finnas tomma platser för ännu oupptäckta element — han förutspådde även egenskaperna hos några av dem, vilket senare bekräftades.
Hur man använder tabellen — praktiska tips
- Identifiera atomnummer för att veta antal protoner och — i neutral atom — även elektroner.
- Titta på gruppnummer för att förutsäga valenselektroner och kemiskt beteende.
- Använd periodnummer för att avgöra hur många elektronskal atomen har.
- Observera block (s, p, d, f) för information om elektronkonfiguration och speciella metalliska egenskaper.
Användningsområden
Det periodiska systemet är ett fundamentalt verktyg inom kemi, fysik, materialvetenskap, biokemi och teknik. Det hjälper forskare och studenter att:
- Förutsäga kemiska reaktioner och bildandet av föreningar.
- Förstå materialegenskaper och utforma nya legeringar eller katalysatorer.
- Söka efter nya, syntetiska element och studera radioaktivitet.
Tillsammans ger alla dessa mönster och indelningar ett kraftfullt sätt att förstå och organisera information om grundämnenas egenskaper och relationer. Det periodiska systemet är därför mer än en tabell — det är ett verktyg för att förutsäga och förklara naturens kemiska beteenden.