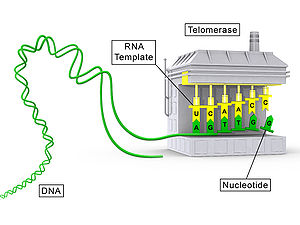
Telomeras är ett RNA-protein och ett enzym som förlänger telomererna genom att lägga till DNA-sekvensrepetitioner (hos ryggradsdjur sekvensen "TTAGGG") i ändarna av kromosomernas DNA. Genom att fungera som en revers transkriptas använder telomeras sin egna RNA-mall för att syntetisera de saknade nukleotiderna i 3'-ändan av telomererna och motverkar därmed gradvis förkortning vid celldelning.
Funktion och mekanism
Telomererna fungerar som engångsbuffertar som skyddar ändarna på eukaryota kromosomer. De består av upprepade, icke‑kodande nukleotid-sekvenser och bindande proteiner som tillsammans förhindrar att kromosomändarna uppfattas som dubbelsträngade brott. På grund av det så kallade slut‑replikationsproblemet förloras 50–200 nukleotider vid varje replikationscykel; detta skadar inte organismens viktigaste genetiska information eftersom telomererna offrar dessa "meningslösa" nukleotider. Telomeras kan dock återställa eller förlänga telomererna i celler där det är aktivt.
Enkelt beskrivet innehåller telomeras en katalytisk proteindel, ofta kallad TERT (telomerase reverse transcriptase), och en RNA-komponent (TERC) som fungerar som mall. TERT adderar nya repetitiva sekvenser i 3'-änden av kromosom-DNA med hjälp av TERC som mall. En rad hjälpproteiner (till exempel dyskerin och andra ribonukleoproteiner) stabiliserar komplexet och reglerar dess aktivitet.
Var i kroppen är telomeras aktivt?
Telomeras är högt aktivt i könsceller, tidiga embryonala celler och många stamcellstyper, där det bibehåller långa telomerer över generationer. Aktivitet kan också ses i aktiverade immunceller (t.ex. vissa lymfocyter). I de flesta terminalt differentierade somatiska celler är telomerasnivåerna låga eller obefintliga, vilket gör att telomererna förkortas med ålder och upprepade celldelningar.
Telomeras, åldrande och sjukdom
Den sovjetiske biologen Alexey Olovnikov förutsade 1973 att en kompensation för telomerförkortning måste finnas och föreslog sambandet mellan telomerförkortning och åldrande samt cancer. Kortare telomerer kopplas till cellulär åldrande (senescens) och nedsatt vävnadsreparationskapacitet. Mutationer i komponenter av telomeras eller associerade proteiner kan leda till ärftliga telomersjukdomar, exempelvis dyskeratosis congenita, som kännetecknas av mycket korta telomerer och organsvikt såsom benmärgssvikt.
Telomeras och cancer
En av de viktigaste kopplingarna till sjukdom är att majoriteten av humana cancerformer återaktiverar telomeras för att bli odödliga — utan aktiverat telomeras skulle tumörceller snabbt nå kritiskt korta telomerer som leder till kromosomal instabilitet, senescens eller apoptos. Över 80–90 % av alla tumörer visar förhöjd telomerasaktivitet, medan en mindre del använder alternativa mekanismer för telomerförlängning (så kallad ALT - alternative lengthening of telomeres).
Förändringar som aktiverande mutationer i TERT-promotorn, amplifikation av TERT-genen eller epigenetiska förändringar kan öka telomerasuttrycket i tumörceller. Detta gör telomeras till ett attraktivt mål för cancerterapi, men också till en utmaning eftersom normal stamcellsfunktion riskerar att påverkas.
Kliniska tillämpningar och forskning
Telomeras är både ett diagnostiskt och terapeutiskt fokus i biomedicinsk forskning:
- Som biomarkör används telomerlängd och telomerasaktivitet för att studera åldrande, vissa genetiska sjukdomar och cancerprognos.
- Terapeutiska strategier i kliniska prövningar inkluderar telomerasinhibitorer (t.ex. oligonukleotider som riktar sig mot TERC eller TERT), immunterapier som riktar immunsvar mot telomerasuttryckta tumörceller, och små molekylär blockering av telomerasfunktion. Ett exempel under utveckling har varit läkemedlet imetelstat.
- Omvänt studeras även kontrollerad aktivering av telomeras som möjlig väg för att förbättra vävnadsreparation eller motverka åldersrelaterad funktionsnedsättning, men detta är förenat med risk för ökad cancerrisk.
Reglering, mätmetoder och alternativa vägar
Telomeras regleras på flera nivåer: transkriptionsnivå (TERT-genens reglering), alternativ splitsning, post‑transkriptionell stabilitet av TERC, proteininteraktioner, och cellulär lokalisering. För att mäta aktivitet i laboratoriet används bland annat TRAP‑assayet (Telomeric Repeat Amplification Protocol) för att detektera telomerasaktivitet, och olika metoder för att mäta telomerlängd (qPCR, Southern blot/Terminal Restriction Fragment, FISH‑baserade metoder).
Vissa celler och tumörer förlänger telomererna utan telomeras genom alternativa homolog rekombinations‑baserade mekanismer (ALT). Dessa skiljer sig molekylärt från telomerasberoende förlängning och kräver särskilda diagnostiska metoder.
Historia och upptäckt
Förekomsten av en mekanism för att motverka telomerförkortning beskrev Alexey Olovnikov 1973. Telomeras upptäcktes experimentellt 1984 av Carol Greider och Elizabeth Blackburn i ciliaten Tetrahymena. Tillsammans med Jack Szostak belönades Greider och Blackburn 2009 med Nobelpriset i fysiologi eller medicin för sina insatser att beskriva telomerernas och telomeras funktion.
Sammanfattningsvis är telomeras ett centralt enzym för kromosomändarnas integritet, med grundläggande betydelse för cellbiologi, åldrande och cancerforskning. Forskning kring telomeras fortsätter att vara intensiv med mål att utnyttja dess egenskaper för diagnostik och behandling, samtidigt som risker kring manipulation av telomeras aktivt beaktas.