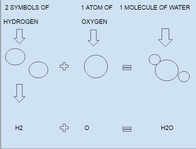
En kemisk formel är ett sätt för kemister att beskriva en molekyl eller ett ämne med hjälp av symboler. Formeln visar vilka atomer som ingår och hur många av varje atomtyp som finns. Ibland visar en formel också hur atomerna är sammankopplade eller hur de är ordnade i rummet.
Bokstaven visar vilket kemiskt grundämne varje atom är. Den nedskrivna siffran (subscript) visar antalet atomer av varje typ. Till exempel har väteperoxid formeln H2O2. Metan har en kolatom (C) och fyra väteatomer; den kemiska formeln är CH4. Sockermolekylen glukos har sex kolatomer, tolv väteatomer och sex syreatomer, så dess kemiska formel är C6H12O6.
Vanliga typer av kemiska formler
- Molekylformel: Visar exakt antal atomer i en molekyl, t.ex. CH4, H2O2, C6H12O6.
- Empirisk formel: Visar förhållandet mellan atomerna i enklaste heltalskvot, t.ex. glukos (C6H12O6) har empirisk formel CH2O.
- Kondensed/strukturell formel: Visar hur atomerna är bundna till varandra i en mer detaljerad form, t.ex. H–O–O–H för väteperoxid eller CH3CH2OH för etanol.
- Strukturformel (Lewis- eller strek-formel): Visar bindningar och fria elektronpar; används för att bestämma molekylens geometri och reaktivitet.
- Jonformel: Visar laddade partiklar, t.ex. NaCl (som jonförening), NH4+, SO42−.
Regler för att skriva formler
- Elementens symboler skrivs med stor begynnelsebokstav och liten andra bokstav (t.ex. C, Cl, Mg).
- Siffror som anger antal atomer skrivs nedsänkta (n). Siffran 1 utelämnas (CH4, inte C1H4).
- Parentheser används runt grupper av atomer när hela gruppen förekommer flera gånger: Ca(OH)2.
- Punkten används för hydrater: CuSO4·5H2O (kopparsulfat-pentahydrat).
- Isotoper anges med massnummer som upphöjt tal framför symbolen, t.ex. 14C för kol-14.
- Laddningar uttrycks som upphöjda tecken: NH4+, Fe2+, SO42−.
Hur formler berättar om struktur och stereokemi
En molekylformel ger bara antal atomer, medan en strukturformel visar bindningsmönster. För att ange tredimensionell ordning används ofta vinklade streck (kil- och strecknotation) eller stereokemiska beteckningar (R/S, E/Z). Till exempel kan två ämnen ha samma molekylformel men olika struktur (isomerer), vilket ger helt olika egenskaper.
Användning i kemi
Kemiska formler används i kemiska ekvationer för att beskriva kemiska reaktioner, räkna stökiometri (hur mycket av varje ämne som krävs eller bildas) och för att identifiera ämnen i laboratoriet, industrin och forskning. Formler är också viktiga för att skriva beräkningar som molantal, koncentrationer och ämnesomsättning i biokemi.
Exempel och tolkning
- CH4 (metan): en kolatom bundet till fyra väteatomer i en tetraedrisk geometri. Enkel molekylgas, viktig som bränsle och råvara.
- H2O2 (väteperoxid): två väte- och två syreatomer. Strukturformeln H–O–O–H visar peroxidbindningen mellan syreatomerna. Väteperoxid används som blekmedel och desinfektionsmedel.
- C6H12O6 (glukos): ett exempel på en kolhydrat. Molekylformeln anger antal atomer, men glukos har flera strukturisomerer (t.ex. aldohexoser) och kan beskrivas mer i detalj med ring- eller kedjestruktur.
Kort historik
Den svenske kemisten Jöns Jacob Berzelius utvecklade under 1800‑talet systemet med elementens symboler och många av konventionerna vi använder än i dag. Hans arbete gjorde kemisk notation enklare, mer standardiserad och lättare att sprida i vetenskapen.
Sammanfattningsvis: en kemisk formel är ett kortfattat sätt att ange vilka atomer som finns i ett ämne och i vilka mängder. För att förstå molekylens egenskaper behöver man ofta komplettera molekylformeln med strukturinformation eller stereokemiska data.