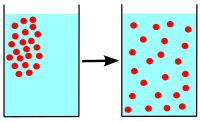
Diffusion är den spontana processen där molekyler eller partiklar rör sig från ett område med hög koncentration till ett område med låg koncentration tills jämvikt uppnås. Rörelsen beror på slumpmässiga kollisioner och termisk rörelse (Brownsk rörelse) hos partiklarna. Diffusion sker i gaser, vätskor och även i fasta material (men mycket långsammare i fasta ämnen) och är en passiv process — den kräver ingen energi eftersom rörelsen sker längs en koncentrationsgradient.
Exempel
- En sockerbit som får ligga i en bägare med vatten löser upp sig och sprids ut i hela vätskan.
- Lukten av ammoniak sprider sig från klassrummets framsida till bakre delen av rummet.
- Parfymdoften stiger upp ur en flaska när locket tas av.
- Livsmedelsfärg som droppas i vatten sprider sig tills färgen är jämnt fördelad.
- Lukten av mat sprids i hela huset genom luften.
På cellnivå tenderar till exempel mer syre att röra sig från en lunga där koncentrationen är hög till blodet där koncentrationen är lägre. På samma sätt rör sig koldioxid från blodet till lungan. Mindre molekyler kan ofta diffundera genom cellmembranet, medan större eller polära molekyler ofta behöver hjälp via kanaler eller transportproteiner (se även aktiv transport och faciliterad diffusion).
Vad påverkar diffusionshastigheten?
Flera faktorer bestämmer hur snabbt diffusion sker:
- Koncentrationsgradienten — större skillnad i koncentration ger snabbare nettotransport.
- Temperatur — högre temperatur ökar partiklarnas kinetiska energi och därmed diffusionshastigheten.
- Medium — diffusion är snabbare i gaser än i vätskor; i fasta material är den mycket långsammare.
- Partikelstorlek — små molekyler diffunderar snabbare än stora.
- Yta — större yta för utbyte ger större flöde av ämnen.
- Avstånd — kortare avstånd gör att diffusion går snabbare; diffusionshastigheten avtar starkt med ökande avstånd.
- Permeabilitet — i biologiska membraner påverkar lipidsammansättning och kanalproteiner hur lätt ett ämne passerar.
Enkel kvantitativ beskrivning (Ficks lag)
Diffusionsflödet kan beskrivas med Ficks första lag i en dimension: J = -D * (dC/dx), där J är flödet (mängd per area och tid), D är diffusionskoefficienten (beroende på ämne och medium) och dC/dx är koncentrationsgradienten. Minustecknet visar att flödet går från hög till låg koncentration. Ficks andra lag beskriver hur koncentrationen förändras över tid vid diffusion.
Yta, volym och biologisk betydelse
I små encelliga organismer räcker ofta enkel diffusion för att byta ut näringsämnen och avfallsprodukter eftersom avstånden är små och förhållandet mellan yta och volym är högt. Ett högt förhållande mellan yta och volym gör att diffusionen kan vara tillräckligt effektiv.
För flercelliga organismer är emellertid enkel diffusion ofta otillräcklig över längre avstånd. Dessa organismer har utvecklat specialiserade transport- och cirkulationssystem för att snabbt förflytta gaser, näringsämnen och avfall. Människan har till exempel lungor med stora ytor och tunna membran som underlättar snabb gasdiffusion mellan luft och blod. I växter bidrar blad och stomata till effektiv gasutbyte och transport i vävnader.
Skillnad mellan diffusion, faciliterad diffusion och aktiv transport
- Diffusion — passiv, sker längs koncentrationsgradienten.
- Faciliterad diffusion — också passiv, men sker via membranproteiner (kanaler eller bärarproteiner) när ämnen inte fritt kan passera lipidmembranet.
- Aktiv transport — kräver energi (vanligtvis ATP) för att flytta ämnen mot en koncentrationsgradient.
Sammanfattning
Diffusion är en grundläggande fysisk process som styr spridningen av molekyler i gaser, vätskor och fasta material. Den är avgörande i många naturvetenskapliga och biologiska sammanhang, från att lösa upp socker i vatten till gasutbyte i lungorna och näringsutbyte i celler. Hur snabbt diffusionen går beror på faktorer som koncentrationsgradient, temperatur, medium, partikelstorlek, yta och avstånd. För större och mer komplexa organismer kompletteras diffusion av specialiserade transportmekanismer för att upprätthålla livsprocesser.