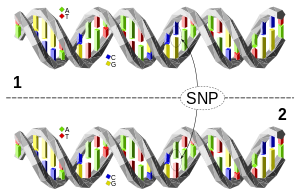
En singelnukleotidpolymorfism (SNP, uttalas snip; plural snips) är en enkelbas‑variation i DNA som förekommer i en population. En SNP är alltså en skillnad i en enda nukleotid i arvsmassan. SNPs är den vanligaste typen av genetisk variation hos människor och används både för grundforskning och tillämpningar inom medicin och rättsmedicin.
Ett enkelt exempel visar hur två sekvenser kan skilja sig med bara en nukleotid: AAGCCTA jämfört med AAGCTTA. I detta fall finns det två alleler för den positionen. I praktiken betraktas en variation som en SNP när den mindre vanliga allelen förekommer med en frekvens på ungefär 1 % eller mer i populationen; mindre frekventa variationer kallas ofta rare variants eller mutationer.
Var i genomet förekommer SNPs och vilka effekter kan de ha?
SNPs finns överallt i genomet, både i kodande (exoner) och icke‑kodande regioner. De flesta vanliga SNPs återfinns i icke‑kodande områden där de sällan påverkar organismens överlevnad — om en variant hade en starkt negativ effekt skulle den ofta rensas bort av det naturliga urvalet. Andra faktorer som genetisk rekombination och mutationshastighet påverkar också hur tätt SNPs förekommer i olika regioner.
Funktionellt kan en SNP ha olika konsekvenser:
- Synonyma förändringar: ändrar nukleotiden utan att ändra aminosyran (ingen direkt effekt på proteinet).
- Missense: ändrar en aminosyra i proteinet, vilket kan påverka dess funktion.
- Nonsense: skapar ett stoppkodon och leder till förkortat protein.
- Splicesite‑SNPs: påverkar splitsningsmönster och kan förändra genuttryck.
- SNPs i regulatoriska element (promotorer, enhancers) kan påverka hur mycket av ett protein som bildas.
Användning i forskning, medicin och rättsmedicin
SNPs fungerar ofta som genetiska markörer. Eftersom de är vanliga och lätt att genotypa används de för att kartlägga arvsgången för egenskaper och sjukdomar, särskilt i genom‑wide association studies (GWAS), där man letar efter SNPs som är statistiskt associerade med en sjukdom eller ett fenotypiskt drag. Viktigt att notera är att en associerad SNP inte nödvändigtvis är orsaken till sjukdomen — den kan sitta i linkage disequilibrium med den verkliga, funktionella varianten.
SNPs har också praktiska tillämpningar:
- Personanpassad medicin och farmakogenetik: vissa SNPs påverkar hur en person svarar på läkemedel (t.ex. varianter i CYP‑gener som påverkar läkemedelsmetabolism).
- Rättsmedicin: SNP‑paneler kan komplettera traditionella STR‑analyser när DNA är kraftigt nedbrutet eller fragmenterat.
- Population/genetisk epidemiologi: SNP‑mönster används för att studera migration, släktskap och befolkningsstruktur.
Ett konkret medicinskt exempel är att en enkelbasmutation i APOE‑genen (apolipoprotein E) är förknippad med en ökad risk för Alzheimers sjukdom. Detta visar hur en enda nukleotidsvariation kan få kliniskt relevanta konsekvenser.
Upptäckt och tekniker
SNPs kan upptäckas och genotypas med flera metoder:
- SNP‑array eller "SNP‑chip" — höggenomiska plattformar som genotypar hundratusentals till miljontals fördefinierade SNPs.
- Next‑generation sequencing (NGS) — ger möjlighet att hitta både kända och nya SNPs över hela genomet eller i utvalda målregioner.
- PCR‑baserade metoder, allelspecifika analyser och Sanger‑sekvensering för validering eller mindre studier.
Population och evolution
SNP‑frekvenser varierar mellan populationer, så en SNP‑allel som är vanlig i en geografisk eller etnisk grupp kan vara mycket ovanligare i en annan. Det gör SNPs användbara för studier av befolkningshistoria och migration. Genom att analysera mönster av SNP‑variation kan forskare identifiera haplotyper (sammansatta varianter som ärvs tillsammans) och områden med låg eller hög rekombination.
Begränsningar och tolkning
Vid tolkning av SNP‑data är det viktigt att komma ihåg:
- En statistisk association innebär inte nödvändigtvis kausalitet.
- Effekterna av en enstaka SNP är ofta små; sjukdomsrisker är vanligtvis multifaktoriella och påverkas av många genetiska varianter och miljöfaktorer.
- Säker och etisk hantering av genetisk information är nödvändig, särskilt i kliniska och rättsmedicinska sammanhang.
Sammanfattningsvis är SNPs enkla men kraftfulla enheter av genetisk variation — viktiga både som biologiska orsaker till variation i egenskaper och sjukdomsrisk, och som praktiska markörer i forskning, medicin och forensik.