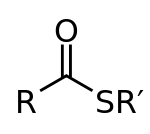
En thioester är en organisk molekyl där en kolylgrupp är bunden till svavel via en C–S–C(O)‑bindning (formellt C–S–CO–C). Strukturellt liknar thioestrar vanliga estrar, men har en svavelatom i stället för syre i den alkoxi-liknande positionen. Likt estrar kan thioestrar framställas från karboxylsyror, men i syntesen används en tiol i stället för en alkohol. Exempel på syntetiska thioestrar är S‑fenyl‑ och S‑etyl‑estern.
Egenskaper och reaktivitet
Thioestrar är generellt mer reaktiva än motsvarande syreatomerade estrar och amider. Anledningen är att svavel inte delokaliserar elektronparet mot karbonylgruppen lika effektivt som syre gör — karbonylkolet blir därför mer elektrofiliskt. Detta gör thioestrar till effektiva acylgivare i många reaktioner och underlättar nukleofil acylsubstitution.
- Hydrolys och energiinnehåll: Thioesterbindningen är lättare att klyva än en vanlig esterbindning, vilket gör att hydrolys ofta frigör mer energi än för en motsvarande syreatomerad ester. Detta är en viktig egenskap i biologiska system.
- Enolisation och kondensationsreaktioner: Thioestrar kan bilda enolater och delta i aldol‑ eller Claisen‑typreaktioner. De används ofta inom organisk syntes som aktiva mellanprodukter vid konstruktion av kol‑kol‑bindningar.
- Trans‑thioesterifiering: Thioestrar deltar lätt i överföring av acylgrupper mellan tioler (transthioesterifiering), vilket är centralt både i syntetisk kemi och i enzymkatalyserade acylöverföringar.
Framställning i laboratorium
Vanliga metoder för att framställa thioestrar inkluderar aktivering av en karboxylsyra (t.ex. med karbodiimider som DCC eller EDC) följt av behandling med en tiol, eller bildning via karboxylklorider (acid chlorides) som reagerar med en tiol. Trans‑thioesterifiering kan också användas för att byta ut en thioestergrupp mellan olika tioler.
Biokemisk betydelse
Thioestrar är mycket viktiga inom biokemin. Ett av de mest kända exemplen är acetyl‑CoA, där acetylgruppen är bunden som en thioester till coenzym A. Acetyl‑CoA fungerar som ett centralt acyl‑donor i många metabolistiska vägar:
- i fettsyrasyntesen som mellanprodukt bärare av aktiva acylgrupper (via acyl‑bärarproteiner och CoA), vilket gör att fettsyror kan byggas upp.
- i citronsyracykeln (TCA‑cykeln) där acetylgruppen från acetyl‑CoA förs in i cykeln och bidrar till ATP‑produktion via oxidativ fosforylering.
- som substrat i olika acyleringsreaktioner, till exempel protein‑acetylering och lipidernas remodeling.
Thioesterbindningens relativt höga fria energi gör att biologiska reaktioner kan drivas framåt när thioestern klyvs — därför fungerar thioestrar ofta som "aktiverade" acyl‑intermediärer i metabolismen och i biosyntetiska processer som leder till ATP och annan energibärande kemi.
Användning inom organisk kemi
I syntetisk kemi används thioestrar som reaktiva elektrofiler och acylbyggstenar. De utnyttjas bland annat i:
- bildning av enolater och subsequent kondensationsreaktioner (t.ex. aldolreaktioner)
- peptidsyntes via native chemical ligation, där en C‑terminal thioester reagerar med en N‑terminal cysteinrest för att skapa en peptidbindning
- selektiva acylöverföringar och i strategi för skydd/grupp‑omvandling i flerstegssynteser
Praktiska aspekter och lukt
Tioxderivat och tioler kan ha starka, ofta obehagliga lukter; vissa thioestrar har däremot fruktiga eller esterlika dofter och används i aromkemi. I laboratoriemiljö bör hantering ske med god ventilation och lämplig skyddsutrustning eftersom vissa tioler och reaktiva mellanprodukter kan vara irriterande eller giftiga.
Sammanfattning
Thioestrar är ersättare till vanliga estrar där syre ersatts av svavel, vilket ger dem ökad reaktivitet och gör dem värdefulla både i biologiska processer (t.ex. acetyl‑CoA och fettsyrasyntes) och i organisk syntes (som aktiva acylkällor och i peptidsyntes). Deras kemiska egenskaper — särskilt den ökade elektrofiliciteten hos karbonylkolet — förklarar varför thioestrar fungerar som effektiva intermediärer i många viktiga reaktioner.