Riktad evolution (DE) är en experimentell metod för att utveckla och optimera enzymer och andra proteiner för industriella, diagnostiska eller medicinska ändamål. Metoden är en form av proteinteknik som efterliknar det naturliga urvalet, men i förkortad och kontrollerad form i laboratoriet.
Grundprincip och arbetsflöde
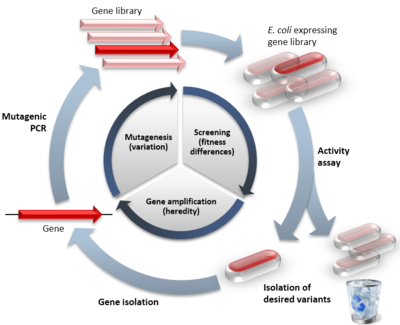
Den grundläggande idén är att en eller flera gener först görs varierade genom upprepade omgångar av mutationer för att skapa ett stort bibliotek av varianter. Biblioteket kan sedan undersökas med hjälp av någon form av urval eller screening för att isolera de varianter som har önskade egenskaper. De bästa varianterna fungerar som en mall för nästa omgång, vilket leder till successiv förbättring över flera cykler.
Skapande av variation
Variation kan introduceras på flera sätt, vanligast är:
- Felintroducerande PCR (error-prone PCR) som ökar mutationsfrekvensen i målgener.
- Siteriktad eller mättad mutagenes där specifika aminosyror eller positionsser ändras systematiskt.
- Rekombination (t.ex. DNA-shuffling) där segment från flera föräldravarianter kombineras.
- Stora syntetiska bibliotek där randomiserade kodon introduceras i utvalda regioner.
Urval och screening
Efter att biblioteket skapats måste funktionellt förbättrade varianter hittas. Det finns två huvudstrategier:
- Selektionsbaserade metoder där endast celler eller partiklar med önskad funktion överlever eller ger ett klart positivt svar. Exempel är kompartmentaliserad självreplikation (CSR) och överlevnadsselektiva system.
- Skärmning där varje variant testas individuellt eller i hög genomströmning för en mätbar aktivitet. Här används ofta flödescytometri (FACS), mikrofluidiska droppar eller automatiserade assays.
In vivo vs in vitro
DE kan utföras antingen in vivo eller in vitro, och båda har för- och nackdelar.
- In vivo: Varianterna uttrycks i levande celler—vanligtvis bakterier eller jäst. I detta fall transformeras varje cell med en plasmid som bär en individuell medlem av variantbiblioteket. Endast målgenen skiljer sig mellan cellerna, medan övriga cellgener är identiska. Proteinet kan uttryckas i cytoplasman eller på ytan, vilket underlättar urval i en cellulär miljö och är särskilt användbart när produkten ska fungera i levande organismer.
- In vitro: Här används cellfria system för transkription och översättning för att producera proteiner eller RNA fritt i lösning eller i konstgjorda mikrodroppar. Fördelarna är bland annat större kontroll över omgivningsparametrar (t.ex. temperatur, lösningsmedel), möjlighet att arbeta med proteiner som är giftiga för celler, och att man kan skapa mycket större bibliotek (upp till 1015) eftersom DNA:t inte behöver införas i celler.
Tekniker för koppling mellan gen och funktion
En viktig del av riktad evolution är att kunna koppla varje genetisk variant till dess funktionella egenskap. Vanliga tekniker är:
- Fagdisplay och yeast display (yt-display) där proteinet knyts till en fysisk partikels yta för selektion.
- Ribosomdisplay och mRNA-display som tillåter urval av bindande eller katalytiskt aktiva varianter helt in vitro.
- Mikrodroppsteknik och droppmikrofluidik för höggenomströmningstester av enstaka gener i separata reaktionskammare.
Tillämpningar och exempel
Riktad evolution används brett:
- För att förbättra industriella enzymer för biokatalys (högre aktivitet, stabilitet vid hög temperatur eller i organiska lösningsmedel).
- Vid utveckling av terapeutiska proteiner och antikroppar med förbättrade bindningsegenskaper eller lägre immunogenicitet.
- För att skapa biosensorer, ny metabolisk aktivitet eller syntetiska biologi‑komponenter.
Metoden belönades delvis med Nobelpriset i kemi 2018 till Frances H. Arnold för utveckling av riktad evolution av enzymer, som illustrerar teknikens betydelse.
Begränsningar, säkerhet och etik
Trots kraften i DE finns begränsningar: experimenten kan vara tids- och resurskrävande, selektionsmetoder måste vara väl utformade för att välja rätt egenskaper, och det finns alltid en risk att förbättring av en egenskap sker på bekostnad av en annan (trade-offs). Säkerhets- och biosäkerhetsfrågor måste också beaktas när man arbetar med genetiskt material och med levande organismer, och regulatoriska krav styr ofta användning och kommersialisering.
Sammanfattning
Riktad evolution är en flexibel och kraftfull metod för att utveckla nya eller förbättrade proteiner genom att kombinera målinriktad variation med selektion eller höggenomströmningstestning. Genom att välja mellan in vivo och in vitro strategier samt genom att använda moderna skärm‑ och displaytekniker kan forskare och industrin skräddarsy proteiner för ett brett spektrum av praktiska användningar.