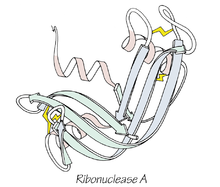
Anfinsens dogm är en hypotes inom molekylärbiologin som föreslogs av Christian Anfinsen. Tanken är att ett proteins veckning till sin ursprungliga struktur sker automatiskt genom proteinets aminosyrasekvens. Det stämmer bara för vissa proteiner. För andra proteiner behövs chaperoner.
Anfinsen delade Nobelpriset i kemi 1972 för sitt arbete med strukturen av enzymet ribonukleas A. Enligt dogmen är den ursprungliga strukturen ett unikt och stabilt tillstånd under de förhållanden där veckningen sker. Det finns tre villkor:
unikhet
kräver att sekvensen inte har någon annan konfiguration med en jämförbar fri energi.
stabilitet
Små förändringar i den omgivande miljön kan inte ge upphov till förändringar i minimikonfigurationen.
kinetisk tillgänglighet
innebär att den slutliga formen kan uppnås utan att man behöver göra några mycket komplicerade ändringar i formen (som t.ex. knutar).
Hur proteinet uppnår denna struktur är ämnet för proteinveckning, som har en relaterad dogm som kallas Levinthals paradox. Levinthals paradox säger att antalet möjliga konformationer som är tillgängliga för ett givet protein är astronomiskt stort, så att även ett litet protein med 100 rester skulle kräva mer tid än vad universum har existerat för att utforska alla möjliga konformationer (10 26sekunder) och välja den lämpliga konformationen.
Prioner är ett undantag från Anfinsens dogm. Prioner är stabila konformationer av proteiner som skiljer sig från det ursprungliga veckningstillståndet. Vid bovin spongiformencefalopati (galna ko-sjukan) omviks de ursprungliga proteinerna till en annan stabil konformation, vilket orsakar dödlig amyloidbildning. Andra amyloidsjukdomar, däribland Alzheimers sjukdom och Parkinsons sjukdom, är också undantag från Anfinsens dogm.
Bakgrund och experimentella bevis
Anfinsens slutsats baserades framför allt på klassiska experiment där ribonukleas A först denaturerades (till exempel med urea och reduktionsmedel) och därefter återfick sin katalytiska aktivitet när denaturerande förhållanden avlägsnades. Detta visade att informationen för att bilda det aktiva, tredimensionella veckade tillståndet låg i aminosyrasekvensen själv, och att disulfidbindningarna i många fall kan formas spontant till sina native-konfigurationer.
Begränsningar och undantag
Anfinsens dogm gäller inte absolut. Några viktiga undantag och förtydliganden:
- Flera proteiner kräver hjälp av molekylära chaperoner (t.ex. Hsp70-familjen, chaperoniner som GroEL/GroES) för att undvika felveckning och aggregation under in vivo‑förhållanden.
- Vissa proteiner veckas cotranslationellt (under syntesen på ribosomen) eller behöver hjälp av enzymatiska processer, t.ex. disulfidisomeraser eller peptidprolylisomeraser.
- Posttranslationella modifieringar, bindning av kofaktorer, metalljoner eller andra subenheter kan vara nödvändiga för att uppnå native‑strukturen.
- Proteiner kan fastna i kinetiska fällor — stabila icke‑native konformationer — som hindrar att den termodynamiska energiminimum uppnås utan assistans.
Levinthal, energifallen och folding‑modeller
Levinthals paradox ledde till utvecklingen av moderna folding‑idéer som "energy landscape" och folding‑trattar: istället för att pröva alla möjliga konformationer rör sig ett veckande protein genom en riktad energimarknad där många vägar leder mot samma globala minimum. Denna modell förklarar hur snabb veckning kan ske trots det astronomiska antalet möjliga konformationer.
Prioner, amyloid och sjukdomar
Prioner är speciella eftersom en felveckad prionform kan fungera som en mall som omvandlar normalt veckade kopior av samma protein till den felveckade formen. Den felveckade formen är ofta rik på beta‑strukturer och bildar fibriller med ett karakteristiskt "cross‑beta"‑mönster. Sådana processer leder till amyloidavlagringar som förekommer vid flera sjukdomar:
- Bovin spongiformencefalopati (BSE) och mänskliga prionsjukdomar (t.ex. Creutzfeldt–Jakobs sjukdom) — smittsamma eller ärftliga prionfenomen.
- Alzheimers sjukdom — associerad med amyloida plack av beta‑amyloid (Aβ) och intraneurala tau‑nystan.
- Parkinsons sjukdom — associerad med aggregation av alfa‑synuklein i Lewykroppar.
- Systemisk amyloidos och lätta kedjeamyloidoser — där olika proteiner eller deras fragment bildar skadliga amyloidfibriller i vävnader.
Tekniker, tillämpningar och medicinska konsekvenser
Studier av proteinveckning och avvikelser därifrån använder bland annat röntgenkristallografi, kärnmagnetisk resonans (NMR), kryo‑EM och molekylärdynamiksimuleringar. Förståelsen av veckningsprinciperna är viktig för:
- utveckling av läkemedel som stabiliserar rätt veckning eller hämmar aggregation,
- design av nya proteiner och enzymer inom syntetisk biologi,
- diagnostik och behandling av amyloidoser och prionsjukdomar, samt
- strategier för att förbättra produktion av rekombinanta proteiner i bioteknik.
Summering
Anfinsens dogm — att aminosyrasekvensen bestämmer ett proteins tredimensionella struktur — var och är en grundläggande idé inom proteinbiokemin. Samtidigt har efterföljande forskning visat att cellulära hjälpmedel, kinetiska effekter, posttranslationella modifieringar och multimerbildning ofta är avgörande för hur proteiner veckas i levande celler. Prioner och amyloidbildning är tydliga exempel där proteiner kan anta andra stabila, men skadliga, konformationer som utgör viktiga undantag till en alltför bokstavlig tolkning av dogmen.