Epigenetik är studiet av förändringar i genaktivitet som inte orsakas av förändringar i DNA-sekvensen. Det handlar om hur samma DNA kan leda till olika celltyper och olika funktioner genom reglering av genuttryck — det sätt på vilket generna åstadkommer sina fenotypiska effekter.
Dessa förändringar i genaktiviteten kan kvarstå under resten av cellens liv och överföra information till många generationer av celler vid celldelning. Det sker dock ingen förändring i organismens underliggande DNA-sekvens. Istället är det icke-ärftliga faktorer och kemiska modifieringar på DNA eller på de proteiner som packar DNA:t som gör att generna uttrycks annorlunda. Ett exempel på en sådan mekanism är DNA-metylering.
Hur epigenetik fungerar
Epigenetiska mekanismer påverkar hur lätt det är för cellens maskineri att läsa av en gen. När en gen är "öppen" kan den transkriberas och producera RNA och protein; när den är "stängd" blir genen tyst. Epigenetiska förändringar är ofta dynamiska — de kan vara stabila över lång tid men ändå reversibla, vilket skiljer dem från permanenta DNA‑mutationer.
Vanliga epigenetiska mekanismer
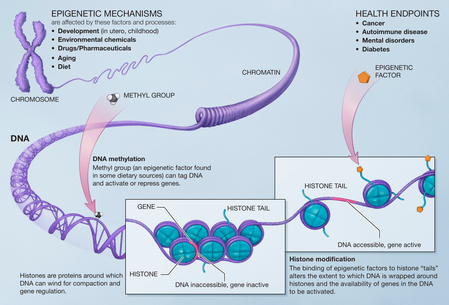
- DNA-metylering — kemisk märkning av DNA (ofta på cytosin‑baser) som vanligen associeras med minskat genuttryck.
- Histonmodifieringar — kemiska förändringar på histonproteiner (t.ex. acetylering, metylering) som påverkar hur tätt DNA är packat och därmed geners åtkomlighet.
- Kromatinremodellering — proteinkomplex som förändrar kromatinets struktur och gör gener mer eller mindre åtkomliga.
- Icke‑kodande RNA (t.ex. mikroRNA, lncRNA) — RNA‑molekyler som inte kodar för protein men kan reglera genuttryck på olika nivåer.
- Genomisk imprinting och X‑inaktivering — speciella fall där endast den maternella eller paternella allelen uttrycks, eller där ena X‑kromosomen i honor stängs av.
Varför epigenetik är viktig
- Cell‑specialisering: Epigenetiska förändringar förklarar hur stamceller kan utvecklas till olika celltyper (t.ex. nervceller, muskelceller) trots att DNA är likadant i alla celler.
- Utveckling och miljö: Faktorer som kost, stress, exponering för kemikalier och tidig livsmiljö kan påverka epigenetiska mönster, ibland redan under fosterstadiet.
- Sjukdom: Störningar i epigenetiska regleringssystem är kopplade till cancer, neurologiska sjukdomar, metabola sjukdomar och vissa utvecklingsstörningar (t.ex. Prader–Willi och Angelman syndrom).
- Åldrande: Epigenetiska förändringar ackumuleras med åldern och används i forskning för att uppskatta biologisk ålder (så kallade epigenetiska klockor).
Exempel och ärftlighet
I vissa fall kan epigenetiska mönster föras vidare över generationer av organismer (transgenerationell epigenetisk ärftlighet), men detta är komplex och varierar mellan arter. Ett ofta citerat exempel i djurförsök är Agouti-musen, där diet under dräktigheten påverkar avkommornas färg och kroppsvikt via DNA‑metylering. Hos människor finns indikationer på att vissa epigenetiska effekter kan påverkas av föräldrars miljö, men graden av ärftlighet och mekanismerna är delvis omstridda och under aktiv forskning.
Metoder för att studera epigenetik
- Bisulfitsekvensering — kartlägger DNA‑metylering på nukleotidsnivå.
- ChIP‑seq — identifierar var specifika histonmodifieringar eller DNA‑bindande proteiner sitter i genomet.
- ATAC‑seq — mäter öppna (åtkomliga) kromatinregioner.
- Andra metoder inkluderar RNA‑seq för icke‑kodande RNA, samt masspektrometri för histonmodifieringar.
Tillämpningar och behandlingar
Eftersom epigenetiska förändringar ofta är reversibla har forskare utvecklat läkemedel som påverkar dessa mekanismer. Exempel är DNMT‑hämmare (som påverkar DNA‑metylering) och HDAC‑hämmare (som påverkar histonacetylering). Sådana läkemedel används eller testas för cancer och andra sjukdomar. Epigenetisk forskning har också betydelse för personlig medicin, där en patients epigenetiska profil kan påverka behandling eller prognos.
Sammanfattning
Epigenetik är läran om hur gener regleras utan att ändra själva DNA‑sekvensen. Genom mekanismer som DNA-metylering, histonmodifieringar och icke‑kodande RNA kan celler styra vilka gener som är aktiva eller tysta. Dessa förändringar spelar en avgörande roll i utveckling, anpassning till miljö, sjukdom och åldrande — och eftersom många epigenetiska markörer är reversibla öppnar de möjligheter för nya behandlingar.