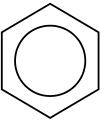
Aromatiska kolväten, ofta kallade arener, är en grupp organiska föreningar karakteriserade av cykliska, konjugerade system där elektroner är delokaliserade över ringen. Termen aromatisk härstammar från att många tidiga upptäckta föreningar hade karakteristisk doft. Den enklaste och mest studerade aromatiska ringen är bensen, en sexledad ring med växelvis dubbel- och enkelbindningar som illustrerar begreppet konjugation och resonans. För en enkel introduktion till grundbegreppet se kolväten och bindningsmönster i aromater via konjugation. Mer om bensen finns under bensenringen.
Egenskaper och teoretisk bakgrund
Aromatisitet är en kvantitativ och kvalitativ egenskap: stabilisering genom delokaliserade π‑elektroner gör aromater mer stabila än motsvarande öppna kedjor. En enkel regel som ofta används är Hückels regel: ett plant, cykliskt, fullt konjugerat systems π‑elektroner ger aromatisk stabilitet när antalet följer 4n+2 (n ett heltal) — se Hückels regel. Detta förklarar varför vissa ringar är aromatiska medan andra är antikonjugerade eller antiaromatiska.
Typer och exempel
Aromatiska föreningar kan delas upp i monocykiska och polycykliska arener (MAH respektive PAH). Vanliga exempel är:
- Bensen och substituerade benzener (t.ex. toluen).
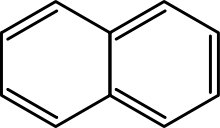
- Polycykliska aromatiska kolväten som naftalen, antracen och fenantren.
- Heteroarener där en eller flera kolatomer ersatts av heteroatomer — exempelvis furan (syre), pyridin (kväve) och tiofen (svavel). Se även syreatomer, kväve och svavel i heterocykliska system.
Förutom neutrala kolväten kan även joner vara aromatiska (t.ex. tropyliumkationen eller cyklopentadienylanjonen) när de uppfyller Hückels kriterier.
Kemiska reaktioner och användningsområden
Aromater deltar i specifika reaktioner som elektrofila aromatiska substitutioner (t.ex. nitrering, sulfonering och halogenering) snarare än i additioner som vanligtvis förstör aromatsystemet. Industriellt är aromatiska kolväten viktiga som lösningsmedel, råmaterial för polymerer, färgämnen, läkemedel och specialkemikalier.
Miljö, hälsa och historik
Bensen är känd för sin toxicitet och klassas som cancerframkallande vid långvarig exponering; polycykliska aromatiska kolväten (PAH) uppkommer vid ofullständig förbränning och kan vara persistenta och miljöskadliga. Historiskt kom namnet "aromatisk" från lukt, men idag används begreppet primärt för att beskriva elektronisk struktur och stabilitet. Strukturbeskrivningar av bensen och begreppet resonans utvecklades under 1800‑talet, bland annat i arbeten av Kekulé; modern kvantkemisk teori ger en djupare förklaring av aromatisk stabilisering.
För vidare fördjupning om särskilda reaktionstyper, säkerhetsaspekter och strukturella varianter finns ämnessidor och läromedel via länkarna ovan.