Det finns fyra vanliga materiatillstånd (eller faser) i universum: fast, flytande, gas och plasma. Ämnestillståndet påverkar ett ämnes egenskaper, t.ex. densitet, viskositet (hur väl det flyter), formbarhet (hur lätt det är att böja) och ledningsförmåga.
Materiens tillstånd
Vanliga materiatillstånd
Fastämnen
I ett fast ämne är atomernas positioner fixerade i förhållande till varandra under lång tid. Detta beror på sammanhållningen eller "friktionen" mellan molekylerna. Denna sammanhållning tillhandahålls av metalliska, kovalenta eller joniska bindningar. Det är bara fasta ämnen som kan tryckas på av en kraft utan att ändra form, vilket innebär att de kan vara motståndskraftiga mot deformation. Fasta ämnen tenderar också att vara tillräckligt starka för att hålla sin egen form i en behållare. Fasta ämnen är i allmänhet tätare än vätskor. Att fasta ämnen blir en gas kallas sublimering.
Vätskor
I en vätska dras molekylerna till varandra tillräckligt starkt för att hålla dem i kontakt, men inte tillräckligt starkt för att hålla en viss struktur. Molekylerna kan ständigt röra sig i förhållande till varandra. Detta innebär att vätskor kan flyta smidigt, men inte lika smidigt som gaser. Vätskor tenderar att ta formen av den behållare som de befinner sig i. Vätskor är i allmänhet mindre täta än fasta ämnen, men tätare än gaser.
Gaser
I en gas är de kemiska bindningarna inte tillräckligt starka för att hålla ihop atomer eller molekyler, och därför är en gas en samling oberoende, obundna molekyler som interagerar huvudsakligen genom kollisioner. Gaser tenderar att ta formen av sin behållare och är mindre täta än både fasta ämnen och vätskor. Gaser har svagare attraktionskrafter än fasta ämnen och vätskor. Att en gas direkt blir fast kallas för avlagring.
Gaser kan ibland omvandlas direkt till fasta ämnen utan att passera genom ett fluidstadium. Detta kallas desublimering. Man kan se det i den frost som bildas på fönsterrutor i kalla klimat. Det är den omvända varianten av sublimering.
Plasma
Plasma är en gas som har så mycket energi att atomens elektroner inte kan hålla sig i omloppsbana runt en atomkärna. Atomjonerna och de fria elektronerna blandas runt som en het soppa.
Eftersom de positivt och negativt laddade partiklarna inte sitter ihop är plasma en bra ledare för elektricitet. Luft är till exempel inte bra på att leda elektricitet. Men i en blixt får atomerna i luften så mycket energi att de inte längre kan hålla fast vid sina elektroner och blir en plasma under en kort stund. Därefter kan en elektrisk ström flyta genom plasman, vilket ger upphov till blixten.
Plasma är det vanligaste materiatillståndet i universum. Både stjärnor och det interstellära mediet består till största delen av plasma.
Fasförändringar
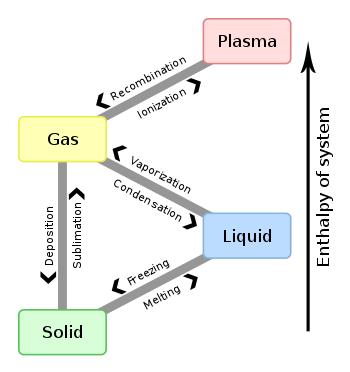
Materiens faser kan förändras på flera sätt. De vanligaste är temperatur och tryck. Ämnen blir vanligen gas vid varma temperaturer och/eller låga tryck, fasta ämnen vid kalla temperaturer och plasma vid extremt varma temperaturer. Ämnen blir ofta flytande mellan fast och gas, men när trycket är mycket lågt (t.ex. vakuumet i yttre rymden) hoppar många ämnen över den flytande fasen och går direkt från fast till gas eller tvärtom. Forskare har skapat grafer som kallas fasförändringsdiagram för att visa förhållandet mellan tryck, temperatur och fas för många ämnen.
När ett fast ämne blir flytande kallas det för smältning. När en vätska blir fast kallas det frysning. När ett fast ämne blir en gas kallas det sublimering. När en gas blir fast kallas det desublimation. När en vätska blir en gas kallas det för avdunstning. När en gas blir en vätska kallas det kondensation.
Fryspunkten och smältpunkten sägs vara desamma, eftersom varje temperaturökning från denna punkt får ämnet att smälta, medan varje temperatursänkning får det att frysa. På samma sätt är förångnings- och kondensationspunkterna (eller sublimerings- och desublimeringspunkterna) alltid lika. I de flesta ämnen ökar förångnings-/kondensationspunkten också när trycket ökar, eller vice versa. Exempelvis sjunker vattnets kokpunkt när man går uppför ett berg, eftersom lufttrycket är lägre. Förhållandet för frysning och smältning kan gå i olika riktningar beroende på ämnet.
Andra stater
Många andra materiatillstånd kan existera under speciella förhållanden, inklusive konstig materia, superolider och möjligen nätvätskor. Forskare arbetar med experiment vid mycket höga eller mycket låga temperaturer för att lära sig mer om materiens faser.
Kondensat
Bose-Einstein-kondensat och fermioniska kondensat är faser av materia som gäller för partiklar som kallas bosoner respektive fermioner. (Mer än en boson kan existera på samma plats samtidigt. Endast en fermion kan existera på samma plats samtidigt). Bose-Einstein-kondensat och fermioniska kondensat förekommer vid otroligt låga temperaturer (ca 4° Kelvin, vilket är detsamma som -452° Fahrenheit). Alla partiklar i dessa kondensat börjar agera som ett enda stort kvanttillstånd, så de har nästan ingen friktion eller elektriskt motstånd.
Degenererad materia
När kärnan i en stjärna får slut på lätta grundämnen (som väte eller helium) för att upprätthålla fusionen, kommer kärnan att kollapsa till ett mycket tätt tillstånd som kallas degenererad materia. Allt är packat mycket tätt och kan knappt röra sig. Om stjärnan inte är för tung blir den en vit dvärg. I en tyngre stjärna är trycket så intensivt att till och med protonerna och elektronerna krossas, och den blir en neutronstjärna.
Kvark-gluonplasma
De protoner och neutroner som utgör atomer består av ännu mindre saker som kallas kvarkar (som "limmas" ihop av saker som kallas gluoner). Vid otroligt höga temperaturer på över 2 biljoner Kelvin omvandlas kvarkar och gluoner till ett annat tillstånd av materia. Människor kan göra lite kvark-gluonplasma i Large Hadron Collider vid CERN, men det håller inte länge innan det svalnar.
Superkritiska vätskor
När ett ämne har tillräcklig temperatur och tryck samtidigt, den så kallade kritiska punkten, kan man inte se skillnad på en mycket tät gas och en mycket energirik vätska. Detta är en superkritisk vätska, och den beter sig som både vätska och gas.
Superfluider
Superfluider uppstår däremot endast vid mycket låga temperaturer och endast för några få speciella ämnen som flytande helium. Superfluider kan göra saker som vanliga vätskor inte kan göra, som att flyta upp på sidan av en skål och komma ut.