SN 2-reaktionen (även kallad bimolekylär nukleofil substitution) är en substitutionsreaktion inom organisk kemi. Det är en typ av nukleofil substitution, där ett ensam par från en nukleofil angriper ett elektronbristande elektrofilcentrum och binder sig till det. Därmed utvisas en annan grupp som kallas "avgångsgrupp". Den inkommande gruppen ersätter alltså den avgående gruppen i ett steg. Eftersom två reagerande arter är inblandade i det långsamma, hastighetsbestämmande steget i reaktionen, leder detta till namnet bimolekylär nukleofil substitution, eller SN 2. Bland oorganiska kemister kallas SN 2-reaktionen ofta för utbytesmekanismen.
Mekanism
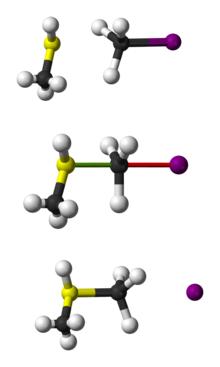
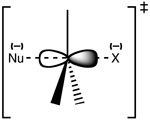
SN2 är en konserted (en-stegs) mekanism där nukleofilen angriper det elektrofila kolatomen från motsatt sida av avgångsgruppen. Detta leder till ett enstegs övergångstillstånd där en delbindning finns både till den inkommande nukleofilen och till avgångsgruppen. När avgångsgruppen lämnar bildas den nya bindningen helt.
Hastighet och kinetik
Reaktionshastigheten för SN2 följer en andragradig kinetik:
- Hastighetslag: rate = k [nukleofil] [substrat]
- Eftersom både nukleofil och substrat deltar i hastighetsbestämmande steget påverkar koncentrationen av båda reaktanter direkt reaktionshastigheten.
Stereokemi
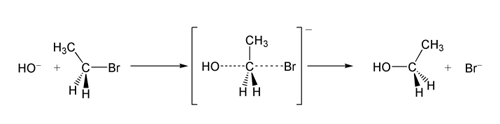
Ett karakteristiskt kännetecken för SN2 är att attacken sker från baksidan i förhållande till avgångsgruppen, vilket ger en inversion av konfigurationen vid det stereocentret. Denna inversion kallas ofta för Walden-inversion. Om substratet är ett kiralt kol får produkten motsatt absolut konfiguration jämfört med utgångsmaterialet.
Faktorer som påverkar SN2
- Substratets struktur: lättast för metyl och primära kol, svårare för sekundära och mycket långsamt eller förhindrat för tertiära på grund av steriskt hinder.
- Avgångsgruppens förmåga: bra avgångsgrupper (t.ex. halider som Br–, I–, eller tosylat) underlättar reaktionen.
- Nukleofilens styrka: starkare nukleofiler (högt elektronpardonerande förmåga) ökar reaktionshastigheten. Laddade nukleofiler (t.ex. OH–, RS–) är ofta mer reaktiva än neutrala (t.ex. H2O).
- Löslighet och lösningsmedel: polära aprotiska lösningsmedel (t.ex. acetonnitril, DMSO, DMF) favoriserar SN2 genom att inte solvatisera nukleofilen starkt, medan protiska lösningsmedel (t.ex. vatten, alkoholer) kan minska nukleofilens reaktivitet genom vätebindning.
- Elektroniska effekter: elektronattraherande substituenter på substratet kan öka elektrofiliciteten och underlätta attacken.
- Temperatur och koncentration: högre temperatur och högre koncentrationer av reaktanter ökar reaktionshastigheten.
Övergångstillstånd och energi
I SN2 finns ett högtordningstillstånd (transition state) där det centrala kolet är delvis bundet till både inkommande nukleofil och avgångsgrupp. Energi- och reaktionsprofilen har en enda energibarriär (en topp) mellan reaktanter och produkter. Steriska hinder och dåliga nukleofiler höjer denna barriär och sänker reaktionshastigheten.
Exempel och tillämpningar
- Ett enkelt exempel är hydrolys av metylbromid med hydroxid: CH3Br + OH– → CH3OH + Br–. Denna går snabbt genom SN2.
- Alkylering av svavel- eller kvävebaser med alkylhalider (t.ex. för att skapa etyl- eller metylderivat) sker ofta via SN2.
- Benzylic och allylic substrat reagerar ofta lätt eftersom övergångstillståndet kan stabiliseras av resonans.
Sammanspel med andra mekanismer
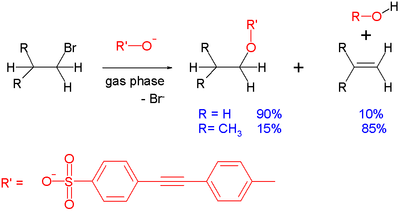
SN2 konkurrerar ibland med andra reaktioner, särskilt SN1 och E2. Vilken mekanism som dominerar beror på substratets struktur, lösningsmedel, temperatur och nukleofilens natur. Till exempel ger tertiära alkylhalider oftast SN1 eller E2 snarare än SN2 på grund av sterisk hindring.
Särskilda effekter och undantag
- Nabo-grupps deltagande: i vissa fall kan intilliggande grupper delta (intramolekylärt) och ändra den förväntade mekanismen.
- Dubbel inversion eller retention: under vissa kontrollerade tvåstegssekvenser kan man få retention av konfiguration genom två på varandra följande inversioner, men en enkel SN2 ger normalt inversion.
Sammanfattningsvis är SN2 en viktig, välkaraktäriserad mekanism i organisk kemi med tydliga kriterier för när den är snabb eller långsam: god nukleofil, bra avgångsgrupp, litet steriskt hinder och lämpligt lösningsmedel främjar reaktionen.