Genterapi innebär att man för in en fungerande gen i en person som har en skadad eller saknad gen. Syftet är att återställa eller förbättra en saknad funktion i kroppen genom att de patientens celler får möjlighet att tillverka ett fungerande protein. Europeiska kommissionen gav 2012 marknadsföringstillstånd för en sådan behandling med produkten Glybera, vilket gjorde den till den första genterapin som godkändes i EU. Tillståndet gjorde det möjligt att sälja behandlingar i hela EU, även om kommersiell användning senare var mycket begränsad och läkemedlet drogs tillbaka av tillverkaren 2017 på grund av bristande efterfrågan.
Hur fungerar virusvektorer?
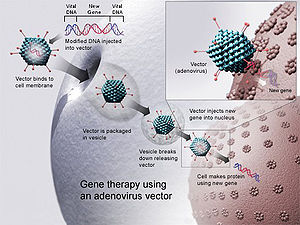
När man använder ett virus för att föra in gener kallas viruset en vektor. Vektorn fungerar som en bärare: forskarna placerar den fungerande genen i virusets arvsmassa och använder virusets naturliga förmåga att ta sig in i mänskliga celler för att föra med sig genen. Om viruset lyckas få in genen i cellens maskineri kommer cellen att börja tillverka det protein som genen kodar för.
I vardagligt bruk talas ibland om transfektion, men när man använder ett virus brukar man mer korrekt tala om transduktion. Skillnaden är att transfektion ofta används när nukleinsyra (DNA eller RNA) förs in med icke-virala metoder, medan transduktion avser överföring med hjälp av ett virus.
Typer av virusvektorer och deras egenskaper
- Adenoassocierade virus (AAV) – används i flera moderna genterapier (inklusive Glybera, som använde AAV-typ 1). AAV integrerar vanligen inte permanent i värdcellens genom utan finns kvar som episomer i cellkärnan, vilket minskar risken för att störa andra gener. De ger oftast måttlig immunreaktion och kan ge långvarig genuttryck i icke-delande celler.
- Adenovirus – kan ge starkt uttryck av den införda genen men ger ofta kraftigare immunsvar. De integrerar normalt inte i värdgenomet.
- Lentivirus (t.ex. HIV-baserade vektorer) – kan integrera i värdcellens genom och ge varaktigt uttryck även i delande celler. Integrationen innebär en risk för insertionell mutagenes (att en gen störs och eventuellt kan bidra till cancer), vilket kräver noggrann design och övervakning.
Ex vivo vs in vivo
Det finns två huvudstrategier för genterapi:
- Ex vivo: Celler tas ut ur patienten, modifieras i laboratorium (vanligt med virala vektorer) och återförs sedan till patienten. Detta används bland annat vid vissa stamcells- och CAR-T-behandlingar.
- In vivo: Vektorn injiceras direkt i patienten (t.ex. i muskel, lever eller blod), vilket är tillvägagångssättet som användes för Glybera (intramuskulär injektion).
Glybera och lipoproteinlipasbrist (LPL-brist)
Runt en av en miljon människor har skadade kopior av genen för lipoproteinlipas (LPL), det enzym som behövs för att bryta ner triglyceridrikt fett i blodet (fett). Sjukdomen leder till mycket förhöjda triglyceridnivåer (kylomikronemi), vilket kan orsaka svåra och upprepade inflammationer i bukspottkörteln (pankreatit) — ett tillstånd som kan vara livshotande. Traditionell behandling har i första hand varit en mycket fettsnål kost och symtomlindring.
Glybera (alipogene tiparvovec) användes för att föra in en fungerande kopia av LPL-genen i muskelceller med hjälp av en modifierad AAV-vektor. Musklerna kan sedan producera lipoproteinlipas som hjälper till att bryta ner blodfetter och därmed minska risken för pankreatit. I kliniska prövningar såg man blandade resultat: vissa patienter fick tydlig nytta medan effekten hos andra var mer begränsad. Dessutom var behandlingen mycket kostsam, vilket bidrog till den begränsade användningen i praktiken.
Säkerhet, risker och reglering
Genterapi har stor potential, men innebär också risker som forskare och myndigheter noggrant övervakar:
- Immunsvar: Kroppens immunförsvar kan känna igen och reagera på både virusvektorn och det nya proteinet, vilket kan minska effekten eller ge biverkningar.
- Insertionell mutagenes: Vissa vektorer som integrerar i genomet kan oavsiktligt störa andra gener och i värsta fall öka risken för cancer. Detta var en verklig fråga i tidiga retrovirusbaserade behandlingar och ligger bakom dagens försiktighet.
- Tillfälligt eller otillräckligt uttryck: Vissa vektorer ger bara kortvarigt genuttryck eller når inte tillräckligt många celler för att ge full effekt.
- Etiska och juridiska frågor: Delning mellan somatisk genterapi (ändringar i kroppsceller som inte ärvs) och germline-genterapi (ändringar som kan ärvas) är viktig. Germlinemodifiering är i praktiken förbjuden i många länder på grund av etiska skäl.
Sammanfattning
Genterapi innebär att man för in en fungerande gen i en person för att behandla en genetisk sjukdom. Virusvektorer är effektiva bärare som kan leverera gener till patientens celler, men olika vektorer har olika egenskaper vad gäller varaktighet, risker och immunsvar. Glybera var ett tidigt exempel på en AAV-baserad genterapi för lipoproteinlipasbrist som fick godkännande i EU, men som i praktiken användes mycket sparsamt på grund av kostnad och blandade behandlingsresultat. Fältet utvecklas snabbt, med förbättrade vektorer och ökad kunskap om säkerhet och effektivitet.