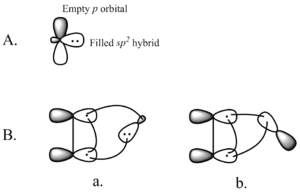
En cheletropisk reaktion är en speciell typ av pericyklisk reaktion där en enda atom i en av reaktanter bildar två nya bindningar samtidigt. Pericykliska reaktioner går via ett övergångstillstånd med en cyklisk uppradning av atomer och överlappande orbitaler, där σ‑ och π‑bindningar omorganiseras i denna cykliska enhet.
Mekanism och egenskaper
Cheletropiska reaktioner är i regel koncertanta (sker i ett stegs mekanism) och involverar en cyklisk övergångstillstånd där båda nya bindningarna bildas eller bryts vid samma atom. Det gör att reaktionen ofta är stereospecifik och styrs av orbitalsymmetrin i övergångstillståndet. En viktig teoretisk ram för att förutsäga om en given cheletropisk process är termiskt tillåten är Woodward–Hoffmann-reglerna (konservering av orbitalsymmetri): beroende på antal involverade elektronpar och hur bindningar bildas kan reaktionen vara suprafacial eller antarafacial.
Skillnad mot andra cycloadditioner
Cheletropiska reaktioner är en underklass av cycloadditioner. Det som särskiljer dem är att båda de nya bindningarna till en av reaktanter görs till samma atom (till exempel en karben‑ eller heteroatom). I många vanliga cycloadditioner binds varje av de två nya σ‑bindningarna till olika atomer på reaktanten, medan cheletropiska reaktioner koncentrerar båda bindningarna till en och samma atom.
Exempel
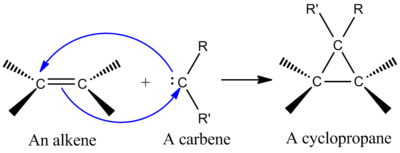
- Cyclopropanering med karbener: Addition av en karben (t.ex. :CH2) till en dubbelbindning är ett klassiskt exempel. Karbenkolet bildar samtidigt två nya σ‑bindningar till de två kolatomerna i alkenet, och produkten blir en cyklopropanring. Detta är en cheletropisk addition eftersom den ena reaktantens (karbenets) single atom får två nya bindningar.
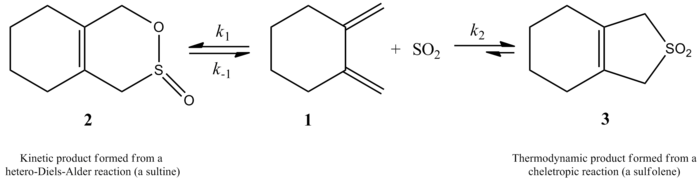
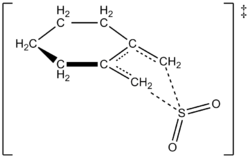
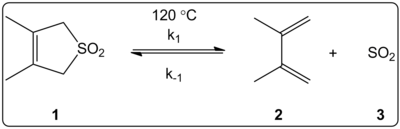
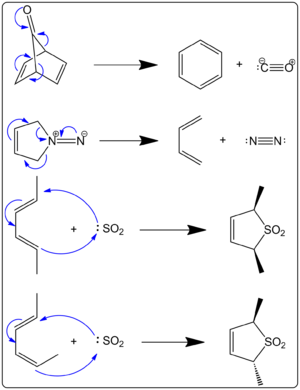
- Cheletropa extrusioner: I vissa retro‑cheletropiska reaktioner frigörs en liten, ofta gasformig molekyl. Exempel är termisk avspjälkning av svaveloxid från sulfolener (ger butadien + SO2) eller andra system där utsläpp av CO eller N2 förekommer. I dessa fall är drivkraften ofta både entalpisk (stabil produkt) och entropisk (frigörelse av en gas), vilket skiftar jämvikten mot produkterna.
- Metallkomplexreaktioner: Vissa reaktioner där en liten ligand (t.ex. CO) avspjälkas eller binds till en metall kan beskrivas i cheletropiska termer när två bindningar bildas eller bryts gentemot samma atom/fragment i ett concerted steg.
Drivkrafter och termodynamik
De viktigaste faktorerna som bestämmer om en cheletropisk reaktion sker är: förändring i bindningsenergi (ΔH), förändring i ordning/antal partiklar (ΔS) och orbitalövergångarnas symmetri. Extrusioner där en gas som CO eller N2 frigörs gynnas ofta starkt av den positiva entropiförändringen. I andra fall kan ringstrain, bildning av aromatiska eller stabila produkter samt elektroniska effekter (elektronfattiga eller -rika centra) vara avgörande.
Stereokemi och experimentell bevisning
Cheletropiska reaktioner är ofta stereospecifika: suprafacial addition till en dubbelbindning leder till retention av konfiguration hos π‑systemet, medan olika topologier i övergångstillståndet kan ge andra utfall. Experimentellt studeras mekanismen med kinetik, isotopmärkning, stereokemiska studier och modernare metoder som beräkningskemi (övergångstillståndsberäkningar) och spektralanalys för att avgöra om reaktionen är concerted eller proceeds via intermediärer.
Sammanfattning
En cheletropisk reaktion är en pericyklisk, ofta concerted omorganisation där en enda atom i en reaktant bildar eller förlorar två bindningar i ett cykliskt övergångstillstånd. De är en viktig undergrupp av cycloadditioner och retro‑cheletropiska extrusioner, och studeras både för sin teoretiska betydelse (orbitalsymmetri, stereokemi) och sina praktiska tillämpningar (t.ex. syntes av cyklopropaner eller termisk eliminering av små gaser).
I figur 1 till höger visas några typiska exempel. I ett av exemplen avges en kolatom som blir kolmonoxid (CO) — i sådana fall talar man ofta om en cheletropisk extrusion där frigörelsen av en gas är en viktig drivkraft. De två första exemplen i figuren är kända som "cheletropa extrusioner" eftersom en liten stabil molekyl avges vid reaktionen.

![{\displaystyle {\frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}}](https://www.alegsaonline.com/image/a02f69dd0783356fbf24499f57d0df29cd264f16.svg)