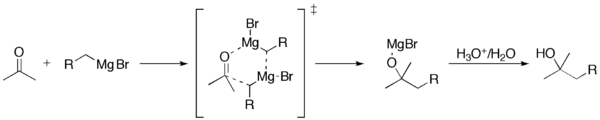
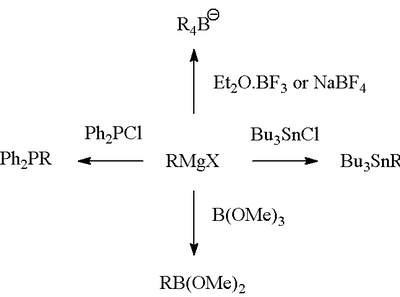
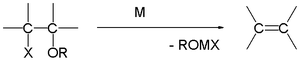
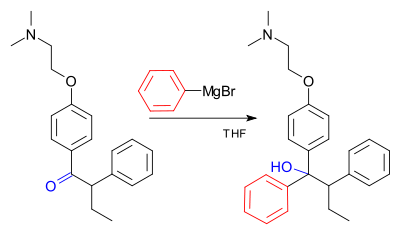
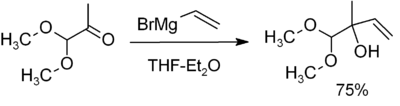Grignardreaktionen (uttalas /ɡriɲar/) är en organometallisk kemisk reaktion där alkyl- eller arylmagnesiumhalogenider (Grignardreagenser) angriper elektrofila kolatomer som finns i polära bindningar (till exempel i en karbonylgrupp som i exemplet nedan). Grignardreagenserna fungerar som nukleofiler. Grignardreaktionen ger upphov till en kol-kol-bindning. Den ändrar hybridiseringen kring reaktionscentrumet. Grignardreaktionen är ett viktigt verktyg vid bildandet av kol-kol-bindningar. Den kan också bilda kol-fosfor-, kol-tin-, kol-silikon-, kol-bor- och andra kol-heteroatombindningar.
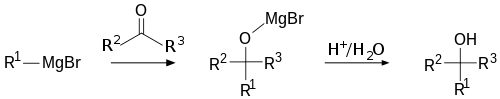
Mekanism och struktur
Grignardreagensen bildas vanligen genom reaktion mellan en alkyl- eller arylhalogenid och metalliskt magnesium i en torr eterlösning (t.ex. dietyleter eller tetrahydrofuran, THF). Den enklaste förenklade beskrivningen är att karbon–halogenbindningen omvandlas till en karbon–magnesiumbindning, RMgX. I verkligheten är dessa ämnen inte rena joner utan förekommer ofta som polymera eller oligomera metallorganiska kluster där eter löser och koordinerar magnesium.
Mekanistiskt kan bildningen av RMgX ske genom en single electron transfer (SET)-liknande process där magnesium överför elektron(er) till organiska halogeniden, vilket ger radikal- och radikal-anjonintermediärer som sedan bildar organomagnesiumföreningen. Inom reaktionen mot en karbonylförening fungerar Grignardreagenset som ett starkt nukleofil som adderar till det elektrofiliska karbonylkolet och bildar först ett alkoxidat (Mg–alkoxid). Efter en syrabehandling (arbetning, "workup") protoneras alkoxidatet och ger motsvarande alkohol.
Vanliga reaktionstyper och användningsområden
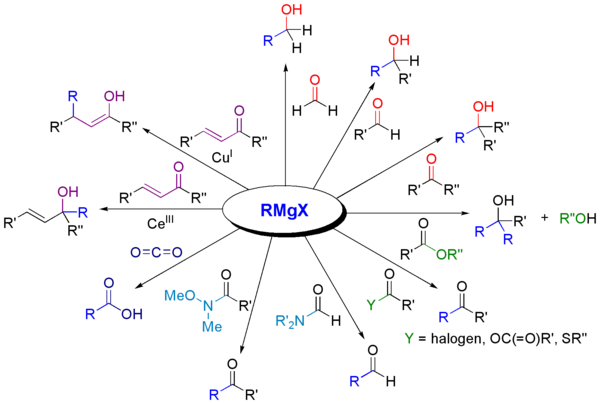
- Tillsats till aldehyder och ketoner → efter syrabehandling ger sekundära eller tertiära alkoholer. Tillsats till formaldehyd ger primära alkoholer.
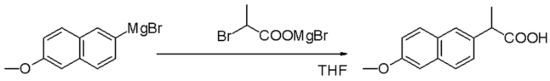
- Reaktion med esterar eller karboxylsyraderivat → oftast två additioner leder till tertiära alkoholer (eftersom intermediatet är en keton som vidare reagerar med Grignardreagenset).
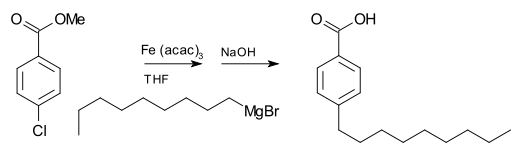
- Reaktion med koldioxid (CO₂) → efter syrabehandling ger karboxylsyror; detta är en vanlig metod att förlänga kolkedjor med en karboxylgrupp.
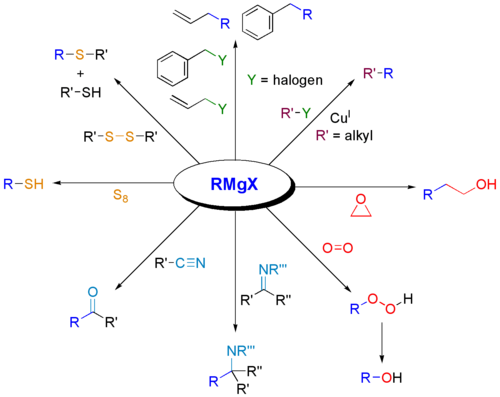
- Öppning av epoxider → ger alkohol med kolkedjeförlängning, attack sker typiskt vid det minst substituerade kolet (under basiska förhållanden).
- Reaktion med nitriler → efter hydrolys ger ketoner.
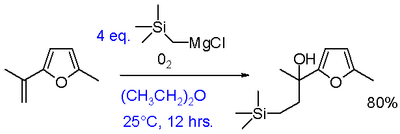
- Bildning av andra C–heteroatombindningar genom reaktion med t.ex. halogenerade fosfor-, silikon- eller borföreningar.
- Industriellt och i totalsyntes används Grignardreagenser ofta för att bygga kolskelet och införliva substituenter selektivt.
Framställning och praktisk hantering
Grignardreagenser framställs vanligen genom omrörning av magnesiumspån eller -flisor med en organisk halogenid i torr eter. Eftersom reagenserna reagerar våldsamt med vatten och protiska lösningsmedel krävs torrt glaskärl och inert atmosfär (kväve eller argon). Vanliga tekniker är att flamtorka eller torka kärlen i ugn och använda Schlenk-teknik eller handskbox (glovebox).
Att sätta igång reaktionen kan ibland kräva aktivering av magnesiumet. Vanliga aktiveringsmetoder är tillsats av en liten mängd jod, 1,2-dibromoetan eller mekanisk/ultraljudsaktivering. Eftersom vissa alkylklorider är tröga kan bromider eller jodider vara att föredra. Ultraljud används ibland för att rengöra/aktivera magnesiumytan som nämnts i originaltexten.
Arbetsupparbetning (quench) måste ske försiktigt eftersom tillsats av vatten eller syra till en lösning innehållande Grignardreagens kan vara mycket exoterma och ge kraftiga reaktioner. Vanligtvis tillsätts en mättad lösning av NH4Cl eller isopropanol långsamt eller man först späder med en inert lösning innan syrabehandling.
Specifika egenskaper och begränsningar
- Funktionell gruppskompatibilitet: Grignardreagenser reagerar omedelbart med alla protiska funktioner: vatten, alkoholer, aminer, karboxylsyror, fenoler och vissa enoleller. Dessa grupper måste skyddas eller elimineras innan användning av Grignardreagens.
- Halt av vatten och luftfuktighet: Luftfuktighet påverkar utbytet vid syntes av RMgX från magnesium och organohalogenid; därför är rigorös uttorkning och inert gas ofta nödvändigt.
- Aggregation och Schlenk-jämvikt: I lösning uppträder Grignardreagenser ofta i aggregerade former och deltar i Schlenk-jämvikter (t.ex. RMgX ⇄ R2Mg + MgX2), vilket påverkar reaktivitet och selektivitet.
- Reaktion med alkylhalogenider: Direkta SN2-kopplingar mellan ett Grignardreagens och en alkylhalogenid är sällsynta på grund av konkurrerande radikalprocesser, eliminering och andra sidoreaktioner. För kopplingsreaktioner används ofta övergångsmetallkatalyserade metoder (t.ex. Kumada‑övergångsmetallkatalys) där Grignard fungerar som nukleofilt organometalliskt reaktant.
- Basstyrka: Grignardreagenser är mycket basiska (deprotonerar lätt substrat med relativt höga pKa-värden). Det höga pKa-värdet för motsvarande alkan (pKa ≈ 45 för en alkan) gör många av dessa reaktioner i praktiken irreversibla och ansvarsfull hantering viktig.
Alternativ och kompletterande metoder
När Grignardreagenser är för reaktiva eller inkompatibla med vissa funktionella grupper finns alternativa organometaller:
- Organolithiumföreningar är ännu mer reaktiva och basiska än Grignardreagenser och används ibland när hög reaktivitet krävs, men kräver ännu strängare anhydra förhållanden.
- Organokopparföreningar (Gilman‑reagenser) är mindre basiska och ger ofta högre selektivitet vid additioner till vissa elektrofiler, t.ex. acylklorider där ketoner kan bildas.
- Övergångsmetallkatalyserade korskopplingar (Kumada-, Negishi-, Suzuki-, Stille-reaktioner) är ofta bättre för att koppla två alkyl-/arylfragment när direkt SN2-koppling med ett Grignardreagens misslyckas.
Säkerhet
Grignardreagenser reagerar lätt med vatten och syre och kan vara pyroforska eller ge brandfarliga metallorganiska produkter vid läckage. Arbeta under inert atmosfär, använd skyddsutrustning och ha rutiner för kontrollerad quench och avfallshantering. Konsultera säkerhetsdatablad (SDS) för specifika reagenser.
Nackdelen med Grignard-reagenserna är att de lätt reagerar med protiska lösningsmedel (t.ex. vatten) eller med funktionella grupper med sura protoner, t.ex. alkoholer och aminer. Luftfuktighet kan ändra utbytet vid framställning av en Grignardreagens från magnesiumspåner och en alkylhalogenid. En av de många metoder som används för att utesluta vatten från reaktionsatmosfären är att flamtorka reaktionskärlet för att avdunsta all fukt, som sedan försluts för att förhindra att fukt återkommer. Kemister använder sedan ultraljud för att aktivera magnesiumets yta så att det förbrukar allt vatten som finns där. På så sätt kan Grignardreagenser bildas med mindre känslighet för vatten.
En annan nackdel med Grignard-reagenserna är att de inte lätt bildar kol-kol-bindningar genom att reagera med alkylhalogenider enligt en SN 2-mekanism.
François Auguste Victor Grignard upptäckte Grignardreaktioner och -reagenser. De är uppkallade efter denna franska kemist (universitetet i Nancy, Frankrike) som fick Nobelpriset i kemi 1912 för detta arbete.