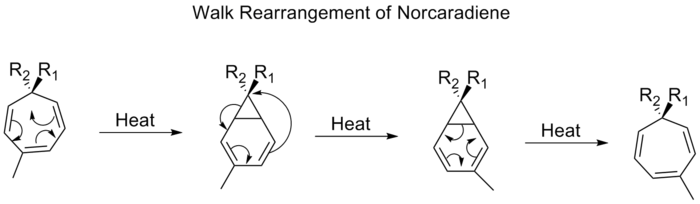
En sigmatropisk reaktion i organisk kemi är en typ av pericyklisk reaktion som normalt sker utan katalysator och intramolekylärt. I en sigmatropisk omarrangering förskjuts en σ-bindning från en position till en annan inom samma molekyl samtidigt som ett π-bundet system omorganiseras. Namnet kommer av ordet "sigma" för enskilda kol–kol-bindningar och det grekiska tropos (vändning). Detta är en omarrangemangsreaktion där inga atomer tillkommer eller lämnar molekylen — i stället flyttas en substituent (eller ett bindningspar) längs ett π-system. Äkta sigmatropa reaktioner behöver vanligtvis ingen katalysator; dock kan vissa underlättas av en Lewis-syra eller av övergångsmetallkatalys. De mest kända sigmatropa omarrangemangen är [3,3]-Cope-omarrangemanget, Claisen-omarrangemanget, Carroll-omarrangemanget och Fischer-indolsyntesen.
Reaktionsmekanism
Sigmatropa reaktioner är pericykliska och ofta concerted — det vill säga alla bindningsomläggningar sker samtidigt via ett cykliskt övergångstillstånd. I ett typiskt fall formas ett aromatiskt eller delokaliserat övergångstillstånd där elektronernas rörelse kan beskrivas som en sluten cykel. Topologin i övergångstillståndet (suprafacialt eller antarafacialt) bestämmer stereokemin och om reaktionen är termiskt tillåten enligt Woodward–Hoffmann-reglerna.
Klassificering och notation
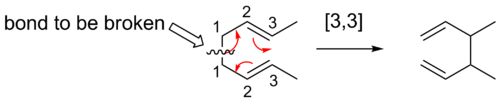
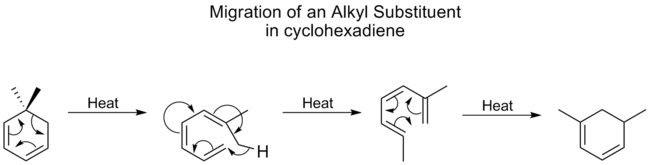
- Sigmatropiska omarrangemang betecknas som [i,j]-skiften, där siffrorna anger hur långt σ-bindningen flyttas i antalet atomer räknat längs respektive del av π-systemet (t.ex. [3,3] för Cope/Claisen).
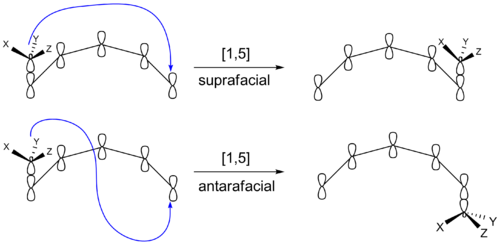
- En förflyttning kan vara suprafacial (migrerande bindning förblir på samma "sida" av π-systemet) eller antarafacial (bindningen rör sig till motsatt sida). Suprafaciala övergångstillstånd är i praktiken vanligare för små till medelstora system eftersom antarafacial geometri ofta är steriskt eller geometriskt omöjlig.
Stereokemi och regler
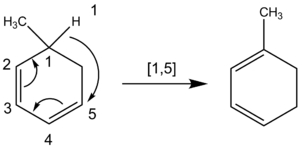
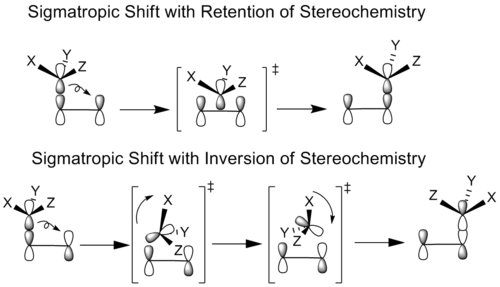
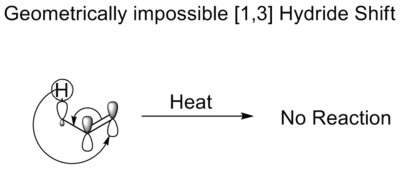
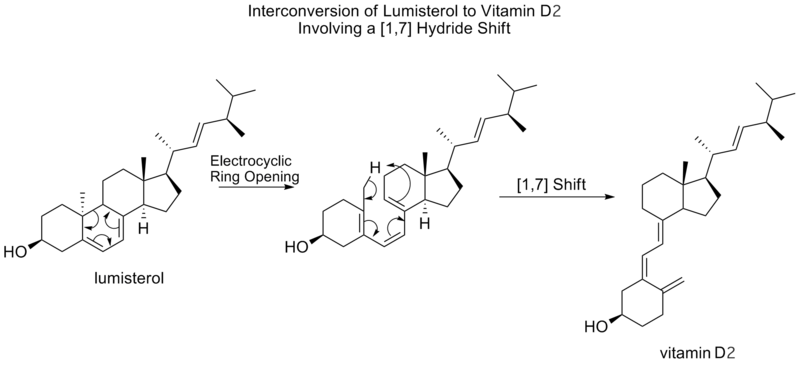
En central aspekt är att sigmatropa reaktioner ofta är stereospecifika. Suprafacial överföring leder typiskt till bibehållen relativ stereokemi (retention) för det migrerande fragmentet, medan antarafacial överföring kan ge inversion. Enligt Woodward–Hoffmann beror termisk tillåtenhet på elektronantalet i det cykliska övergångstillståndet — många vanliga [3,3]- och [1,5]-skiften är termiskt tillåtna och sker suprafacialt, medan exempelvis enkla [1,3]-skiften ofta är missgynnade i små system och i praktiken kan gå via stegvisa radikal- eller jonmekanismer istället. Fotokemiska förhållanden kan ändra dessa tillåtlighetsvillkor och göra andra topologier möjliga.
Viktiga exempel
- Cope-omarrangemanget ([3,3]) — en klassisk omarrangering av 1,5-diener där en σ-bindning flyttas och π-systemet omorganiseras. Reaktionen är vanligtvis reversibel och drivs ofta av termodynamiska faktorer (t.ex. stabilisering genom konjugation eller substitutionsmönster). Enkelt exempel är omvandlingen av 1,5-hexadien-3,4-diolderivat.
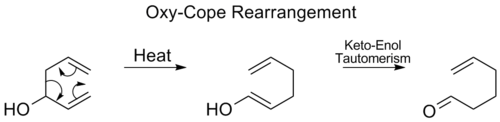
- Oxy-Cope — en variant av Cope där en hydroxy-substituerad 1,5-dien via baskatalys eller upphettning bildar en anionisk intermediär som tautomeriserar till ett karbonylförening (ofta drivande steg) — mycket användbar i syntes.
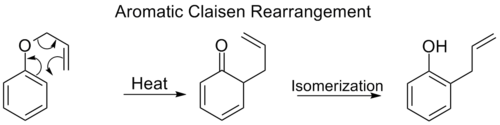
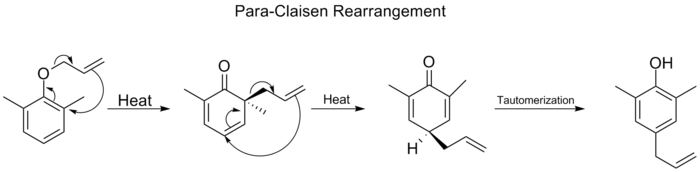
- Claisen-omarrangemanget ([3,3]) — omarrangemang av allyl-vinyletrar till γ,δ-osatunsaturated ketoner eller aldehyder (efter tautomerisering). Många varianter finns: Johnson-, Ireland- och Eschenmoser–Claisen är vanliga modifieringar som ökar funktionell gruppkompatibilitet eller stereokontroll.
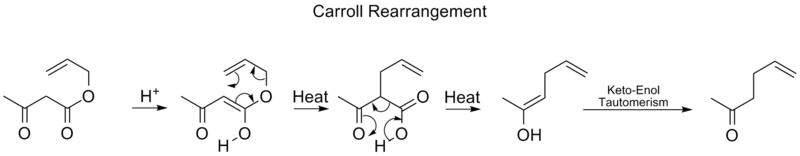
- Carroll-omarrangemanget — en termisk [3,3]-omarrangering av allylcarbonylföreningar (ofta av β-ketoestertyp) som kan åtföljas av decarboxylering för att ge konjugerade produkter; användbar vid ombyggnad av kolkedjor.
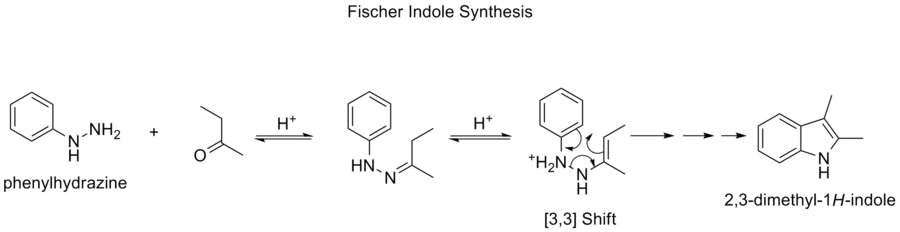
- Fischer-indolsyntesen — en mångstegsprocess där en viktig stegvis sigmatropisk omarrangering kan förekomma (ofta beskriven som en [3,3]-liknande omdisponering) under bildningen av indolringen från fenylhydrazoner och aldehyder/ketoner.
Praktiska och syntetiska aspekter
- Sigmatropa reaktioner används flitigt i syntes av naturliga produkter och i konstruktion av komplexa kol-skelett tack vare deras förmåga att flytta substituenter och bygga eller omstrukturera konjugerade system stereospecifikt.
- Reaktionens reversibilitet (t.ex. i Cope) gör att produktens termodynamiska stabilitet ofta avgör utbyte; därför används ofta drivande steg som tautomerisering (oxy-Cope) eller förlust av koldioxid (Carroll) för att styra reaktionens förlopp.
- Även om många sigmatropa omarrangemang är termiskt tillåtna kan Lewis-syror eller övergångsmetaller ändra mekanism eller sänka aktiveringsenergin genom att koordinera till substratet och skapa alternative, ofta icke-koncerted, vägar.
Sammanfattning
Sigmatropiska reaktioner är en viktig klass av pericykliska omarrangemang som möjliggör förflyttning av σ-bindningar inom molekyler och ombyggnad av π-system på ett stereospecifikt sätt. De mest använda exemplen är [3,3]-omarrangemangen som Cope och Claisen, och reaktionernas termiska tillåtlighet och stereoutfall styrs av övergångstillståndets topologi och Woodward–Hoffmann-principerna. Genom varianter och katalysatorer kan dessa reaktioner anpassas till en rad syntetiska behov och utgör därmed viktiga verktyg i modern organisk syntes.

![[1,3] Alkyl Shifts](https://www.alegsaonline.com/image/550px-1,3alkylfixed.png)
![[1,5] Hydride shift in a cyclic system](https://www.alegsaonline.com/image/300px-1,5hydridecyclicfixed.png)
![Antarafacial [1,5] Hydride Shift](https://www.alegsaonline.com/image/600px-1,5hantarafacialfixed.png)


![[5,5] shift of phenyl pentadienyl ether](https://www.alegsaonline.com/image/800px-5,5shiftfixeds.png)