Gaskromatografi-masspektrometri (GC-MS) kombinerar egenskaperna hos gas-vätskekromatografi (GC) och masspektrometri (MS). Detta gör det möjligt att identifiera olika ämnen i ett testprov. GC-MS har många användningsområden, t.ex. narkotikadetektion, brandutredningar, miljöanalyser och sprängämnesutredningar. Den kan också användas för att identifiera okända prover. GC-MS kan också användas inom flygplatssäkerheten för att upptäcka ämnen i bagage eller på människor. Dessutom kan GC-MS identifiera spårämnen i försämrade material, även efter att provet fallit sönder så mycket att andra tester inte kan fungera.
GC-MS är det bästa sättet för kriminaltekniska experter att identifiera ämnen eftersom det är ett specifikt test. Ett specifikt test identifierar positivt den faktiska förekomsten av ett visst ämne i ett visst prov. Ett ospecifikt test säger bara att kategorier av ämnen finns i provet. Även om ett ospecifikt test statistiskt sett kan ge en antydan om ämnets identitet kan detta leda till falskt positiv identifiering.
Principen i korthet
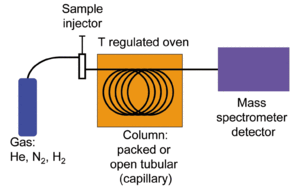
GC-MS består av två huvuddelar:
- Gaskromatografidelen (GC) separerar en blandning i en serie av komponenter genom en kolon (vanligtvis en kapillärkolonn) där olika ämnen eluerar vid olika tider (retentionstider).
- Masspektrometridelen (MS) joniserar de separerade molekylerna och mäter massor och fragmentmönster. Resultatet är en massespektrum som fungerar som ett ”fingeravtryck” för varje ämne.
Instrumentkomponenter och vanliga varianter
- Injektionssystem: Man kan använda split/splitless, pulsat injektion, headspace eller termisk avdunstning beroende på provtyp.
- Kolonn: Olika stationära faser (polära eller icke-polära) ger olika separationsegenskaper. Kapillärkolonner är vanligast.
- Joniseringsmetoder: Elektronjonisation (EI) är standard och ger reproducerbara fragmentmönster, medan kemisk jonisation (CI) ger mjukare jonisering och ofta molekyljon.
- Massanalysatorer: Kvadrupol, Fourier-transform (FT), time-of-flight (TOF) och ionfälla har olika fördelar vad gäller känslighet, massupplösning och hastighet.
- Detektorer och datorsystem: Systemet samlar in kromatogram och spektra, gör bibliotekssökningar och kvantifiering.
Provberedning
Provberedning är ofta avgörande för ett bra resultat. Vanliga tekniker:
- Extraktion: Flyktiga ämnen kan hämtas med lösningsmedelsextraktion, medan andra kräver fastfasextraktion (SPE).
- Headspace- och SPME (solid phase microextraction) är vanliga för flyktiga och semi-flyktiga ämnen (t.ex. dofter, lösningsmedel, brandacceleranter).
- Purge-and-trap används för att koncentrera mycket flyktiga ämnen.
- Derivatisering: Icke-flyktiga eller termiskt instabila föreningar kan kemiskt modifieras (t.ex. silylering) för att bli GC-kompatibla.
Tolkning av resultat
- Kromatogram: Visar retentionstid för varje komponent—användbart för att separera blandningar.
- Masspektrum: Fragmentmönstret jämförs ofta mot bibliotek (t.ex. NIST) för identifiering. Bibliotekssökning ger ofta en matchningspoäng men måste tolkas kritiskt.
- Kvantifiering: Kräver kalibreringskurvor och interna standarder för noggrann mätning av koncentrationer och gränser för detektion (LOD/LOQ).
- Säker identifiering: För rättsliga eller regulatoriska ändamål används ofta jämförelse med referensstandarder för att bekräfta identiteten.
Tillämpningar och exempel
- Rättsmedicin och kriminalteknik: Identifiering av narkotika (t.ex. kokain, heroin), giftiga ämnen, brandacceleranter (t.ex. bensin, terpentin) och sprängämnesrester.
- Miljöanalys: Bestämning av pesticider, PCB, polyaromatiska kolväten (PAH) och andra organiska föroreningar i vatten, jord och luft.
- Livsmedelsanalys: Spårning av kontaminanter, aromkomponenter och rester av bekämpningsmedel.
- Industri och materialanalys: Identifiering av förfallna bindemedel, plaster och nedbrytningsprodukter.
- Flygplatssäkerhet: Spårdetektion av explosiva ämnen eller kemikalier i bagage och på personer.
Styrkor
- Hög selektivitet och specificitet: kombinationen av separation och massespektrum minimerar falska träffar.
- Mycket känsligt: spårmängder kan ofta detekteras och kvantifieras.
- Bredt användningsområde: många organiska ämnen kan analyseras efter rätt provberedning.
Begränsningar och fallgropar
- GC kräver att ämnen är flyktiga och termiskt stabila eller kan göras det genom derivatisering. Stora, polära och termolabila molekyler kan kräva andra tekniker (t.ex. LC-MS).
- Isomerer och starkt sameluerande komponenter kan vara svåra att skilja utan mycket bra separation eller kompletterande analys.
- Bibliotekmatchningar kan ge falska positiva resultat om inte retentionstider och referensstandarder också kontrolleras.
- Matris- och interferenseffekter kan påverka kvantifiering om inte interna standarder och lämplig rensning används.
Kvalitetssäkring och juridiska aspekter
För rättsmedicinska och regulatoriska analyser är följande viktigt:
- Validering av metoder (precision, noggrannhet, specificitet, LOD/LOQ).
- Spårbarhet och kvalitetssystem (t.ex. ackreditering enligt ISO-standarder).
- Dokumenterad kedja av bevis (chain of custody) och användning av kalibreringsstandarder.
Exempel på arbetsflöde (förenklat)
- Insamling och dokumentation av prov.
- Provberedning (val av extraktion, eventuellt derivatisering).
- GC-separation och MS-analys (val av joniseringsmetod/analysator).
- Spektrumsökning mot bibliotek och jämförelse med referensstandard.
- Kvantifiering med kalibreringskurvor och rapportering av osäkerhet.
Sammanfattning
GC–MS är en mycket kraftfull och mångsidig analytisk teknik som kombinerar separation och strukturell information. Den är särskilt värdefull inom kriminalteknik, miljöövervakning, livsmedelskontroll och andra områden där man behöver identifiera och kvantifiera organiska ämnen i komplexa matriser. Rätt provberedning, metodval och kritisk tolkning av masspektrum är avgörande för att få tillförlitliga resultat.